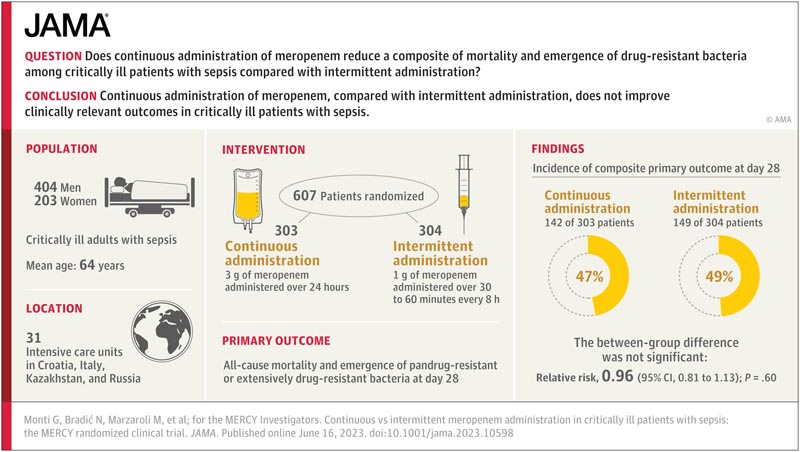
Points clés L’administration continue de méropénem réduit-elle une combinaison de mortalité et d’émergence de bactéries résistantes aux médicaments chez les patients gravement malades atteints de sepsis par rapport à une administration intermittente ? Résultats Dans cet essai clinique randomisé portant sur 607 patients gravement malades souffrant de sepsis ou de choc septique, l’administration continue de méropénème, par rapport à l’administration intermittente, n’a pas diminué de manière significative le composite de mortalité toutes causes confondues et l’émergence de bactéries pan-résistantes ou extrêmement résistantes aux médicaments. au jour 28 (47 % contre 49 %, respectivement). Signification L’administration continue de méropénem, par rapport à l’administration intermittente, n’améliore pas les résultats cliniquement pertinents chez les patients gravement malades atteints de sepsis. |
Importance
Le méropénème est un antibiotique β-lactamine largement prescrit. Le méropénem présente une efficacité pharmacodynamique maximale lorsqu’il est administré par perfusion continue pour délivrer des niveaux de médicament constants supérieurs à la concentration minimale inhibitrice. Par rapport à l’administration intermittente, l’administration continue de méropénème peut améliorer les résultats cliniques.
But
Déterminer si l’administration continue de méropénem réduit une combinaison de mortalité et d’émergence de bactéries pan- ou extrêmement résistantes aux médicaments par rapport à l’administration intermittente chez les patients gravement malades atteints de sepsis.
Conception, environnement et participants
Un essai clinique randomisé en double aveugle recrutant des patients gravement malades atteints de sepsis ou de choc septique à qui leur médecin traitant avait prescrit du méropénem dans 31 unités de soins intensifs de 26 hôpitaux de 4 pays (Croatie, Italie, Kazakhstan et Russie). Les patients ont été recrutés entre le 5 juin 2018 et le 9 août 2022, et le suivi final de 90 jours s’est achevé en novembre 2022.
Interventions
Les patients ont été répartis au hasard pour recevoir une dose égale de l’antibiotique méropénème par administration continue (n = 303) ou par administration intermittente (n = 304).
Principaux résultats et mesures
Le critère de jugement principal était un composite de mortalité toutes causes confondues et d’émergence de bactéries pan- ou extrêmement résistantes aux médicaments au jour 28.
Il y a eu 4 critères de jugement secondaires , y compris les jours en vie sans antibiotiques au jour 28, les jours en vie et sans soins intensifs au jour 28 et la mortalité toutes causes confondues au jour 90. Les convulsions, les réactions allergiques et la mortalité ont été enregistrées comme indésirables. événements.
Résultats
Les 607 patients (âge moyen : 64 [ET, 15] ans ; 203 étaient des femmes [33 %]) ont été inclus dans la mesure du critère de jugement principal de 28 jours et ont complété le suivi de mortalité de 90 jours. La majorité (369 patients, 61 %) présentaient un choc septique.
Le délai médian entre l’admission à l’hôpital et la randomisation était de 9 jours (IQR, 3 à 17 jours) et la durée médiane du traitement par le méropénème était de 11 jours (IQR, 6 à 17 jours). Un seul événement croisé a été enregistré.
Le critère de jugement principal est survenu chez 142 patients (47 %) dans le groupe continu et 149 patients (49 %) dans le groupe intermittent (risque relatif, 0,96 [IC 95 %, 0,81-1,13]. ], P = 0,60).
Sur les 4 critères de jugement secondaires, aucun n’était statistiquement significatif. Aucun événement indésirable, comme des convulsions ou des réactions allergiques liées au médicament à l’étude, n’a été signalé.
À 90 jours, la mortalité était de 42 % dans le groupe d’administration continue (127 sur 303 patients) et dans le groupe d’administration intermittente (127 sur 304 patients).
Discussion
Dans cet ECR international en double aveugle portant sur des patients gravement malades atteints de sepsis, il n’y avait aucune différence significative dans le résultat composite de la mortalité toutes causes confondues et de l’émergence de bactéries pharmacorésistantes ou extrêmement résistantes aux médicaments à 28 jours pour une administration continue par rapport à une administration intermittente. du méropénem. Aucune différence significative n’a été observée pour aucun des quatre critères de jugement secondaires ou pour les éléments individuels du résultat principal composite.
Les résultats de la présente étude suggèrent que l’administration continue de méropénem n’améliore pas les résultats cliniquement pertinents chez les patients gravement malades atteints de sepsis, y compris la mortalité à long terme.
Des études antérieures ont montré des bénéfices en matière de survie à court terme, tandis qu’une étude rapportant une mortalité à 90 jours a montré une différence non significative (26 % dans le groupe continu contre 28 % dans le groupe intermittent, P = 0,67), 40 ce qui est cohérent avec l’étude actuelle. (42% dans les deux groupes, p = 0,97).
Les experts ont en outre suggéré que la méthode d’administration du méropénem devrait prendre en compte d’autres facteurs, tels que la faisabilité, la disponibilité d’une ligne intraveineuse, les problèmes de stabilité du médicament, les coûts et les problèmes logistiques. 45Par ailleurs, les experts ont indiqué qu’aucun sous-groupe spécifique n’a pu être identifié dans lequel l’administration continue pourrait être la cible de futurs ECR.
Conclusions et pertinence
Chez les patients gravement malades atteints de sepsis, par rapport à l’administration intermittente, l’administration continue de méropénem n’a pas amélioré le résultat composite de la mortalité et de l’émergence de bactéries pan- ou extrêmement résistantes aux médicaments au jour 28.
Enregistrement de l’essai : ClinicalTrials.gov Identifiant : NCT03452839















