L’érythromélalgie (EM) est une maladie débilitante rare caractérisée par des épisodes de douleur brûlante associés à des pieds et parfois des mains rouges et chauds.
Pendant les symptômes, les pieds et les mains peuvent être enflés, bien que l’œdème ne soit pas universellement présent ou signalé.
Le contrôle endogène de la température, probablement par vasodilatation des anastomoses artério-veineuses thermorégulatrices, peut être un facteur clé dans le mécanisme physiopathologique de l’érythromélalgie (EM). Les épisodes sont souvent déclenchés par une activité physique et une exposition à des températures chaudes, tandis que la douleur est généralement soulagée en refroidissant les zones touchées.
Étant donné que les symptômes sont intermittents et que les pieds et les mains peuvent sembler normaux lors de la présentation, le diagnostic peut être manqué. Les patients recherchent souvent des soins dans diverses spécialités, notamment les soins primaires, la dermatologie, la médecine vasculaire, la neurologie et le traitement de la douleur. Les patients ont une qualité de vie inférieure, une morbidité et une mortalité accrues ainsi qu’un risque de suicide accru par rapport à la population générale américaine.
Un traitement efficace pour soulager les symptômes est essentiel pour éviter des complications graves et améliorer les résultats. Pour nommer la maladie, il existe des termes tels que SEP primaire et SEP secondaire, mais leur utilisation est variée et peut prêter à confusion.
Classiquement, le terme érythromélalgie secondaire est utilisé pour désigner la SEP dont la cause sous-jacente est identifiable. Le terme SEP primaire est utilisé pour désigner la SEP sans cause sous-jacente identifiable (SEP idiopathique). Le terme SEP primaire a également été utilisé comme synonyme de SEP héréditaire pour décrire la SEP chez les patients ayant des antécédents familiaux de cette maladie. Cependant, qualifier la SEP de primaire ou de secondaire n’affecte pas grandement sa gestion.
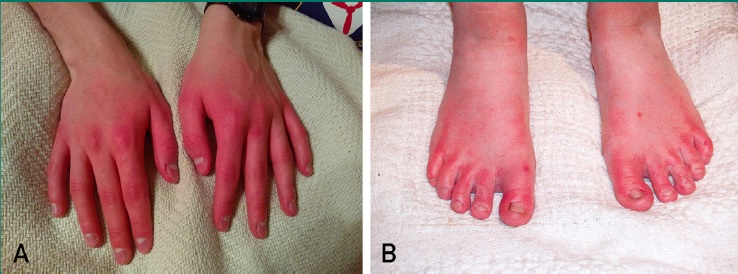
Mains et pieds lors d’un épisode d’érythromélalgie. Les mains (A) et les pieds (B) peuvent être rouges, douloureux et chauds.
| Érythromélalgie primaire |
Environ 5 % des patients ont des antécédents familiaux de SEP, et beaucoup ont une transmission autosomique dominante.
Dans des études portant sur des familles atteintes de SEP autosomique dominante, une variante a été décrite dans la séquence du gène SCN9A, caractérisée par le codage de la sous-unité Nav1.7 des canaux sodiques neuronaux, située préférentiellement dans les ganglions sympathiques et les neurones sensoriels nociceptifs des ganglions. racine dorsale.
La variante séquentielle, une variante à gain de fonction, permet aux canaux sodiques neuronaux Nav1.7 de s’ouvrir plus facilement et de rester ouverts, conduisant à une activation multiple et prolongée de ces neurones sensoriels. Cela aide à expliquer la douleur disproportionnée ressentie par les patients lors des épisodes de SEP. S a rapporté que cette variante à gain de fonction de Nav1.7 produit une hypoexcitabilité des neurones sympathiques.
L’histoire naturelle de la SEP primaire a été bien caractérisée à partir d’une série relativement importante de 13 patients atteints de SEP primaire et de variantes de séquence SCN9A. Près d’un tiers des crises de douleur n’avaient aucun déclencheur identifiable et la plupart des patients ressentaient de la douleur entre les crises.
La SEP a été considérée comme la première neuropathie douloureuse héréditaire connue au niveau moléculaire et comme modèle de maladie, ce qui pourrait être instructif pour d’autres affections douloureuses. Cependant, la SEP familiale n’est pas toujours liée au SCN9A. Par exemple, aucun variant SCN9A n’a été détecté chez un parent de troisième génération atteint de SEP primaire, ce qui suggère qu’un autre gène pourrait également être lié à ce trouble.
| Érythromélalgie secondaire |
De nombreuses associations entre la SEP et des troubles sous-jacents ont été décrites, mais il n’est pas clair si la SEP est véritablement secondaire à ces troubles. Environ 5 % des patients atteints de SEP souffrent d’une maladie myéloproliférative (p. ex. thrombocytémie essentielle et polyglobulie rubra vera).
Chez ces patients, la prise en charge des aspects microvasculaires de la SEP peut être importante, étant donné que la SEP associée à une maladie myéloproliférative est plus susceptible de répondre à l’aspirine .
Des associations avec des maladies auto-immunes sous-jacentes et d’autres troubles ainsi qu’avec des médicaments ont été décrites, mais sont beaucoup moins cohérentes.
| Association avec la neuropathie |
Il existe des preuves d’une association étroite entre la SEP et la neuropathie des petites et des grosses fibres.
Près de 50 % des patients atteints de SEP présentent une neuropathie à grosses fibres lors d’électromyogrammes et d’études de conduction nerveuse.
La présence d’une neuropathie à petites fibres est déterminée par une évaluation fonctionnelle des petites fibres à l’aide de tests de sueur, notamment le test de thermorégulation de la sueur et le test quantitatif du réflexe axonal sudomoteur.
Les tests de thermorégulation de la sueur montrent des anomalies marquées chez environ 90 % des patients. Ce test est une excellente mesure de la neuropathie sensorielle des petites fibres de la peau, puisque les glandes sudoripares sont médiées par de petites fibres nerveuses. Les tests des petites fibres ont également révélé une altération de la fonction des petites fibres chez les patients atteints de SEP.
Il convient de noter que les résultats des biopsies cutanées (souvent utilisées pour diagnostiquer la neuropathie des petites fibres) sont généralement non spécifiques et montrent une diminution de la densité des fibres nerveuses épidermiques dans une minorité de cas seulement. On ne sait pas exactement si la neuropathie conduit à la SEP ou vice versa. les neuropathies des petites fibres pourraient précipiter la SEP. À l’inverse, une maladie sous-jacente comprenant une hyperexcitabilité Nav1.7 et un traitement à l’eau froide peut également conduire à une neuropathie des petites fibres.
| Stratégies de gestion non pharmacologique |
Les symptômes de brûlure associés à des épisodes de rougeur des extrémités peuvent dominer la vie des patients qui tentent d’éviter les situations qui exacerbent leur douleur, et la SEP peut évoluer vers un syndrome de douleur chronique débilitante.
Pour aider les patients à éviter cette progression, il leur est conseillé de ne pas abandonner leur mode de vie habituel, en cherchant à éviter ou à minimiser autant que possible les déclencheurs connus. Pour ce faire, ils doivent recevoir des conseils sur les recommandations en matière de mode de vie afin de minimiser les épisodes de SEP et les symptômes associés. Ces stratégies sont particulièrement utiles car elles peuvent réduire le besoin de traitements pharmacologiques et interventionnels.
Les patients doivent apprendre à contrôler la douleur avec des médicaments topiques et systémiques ; pour résoudre les problèmes psychologiques associés, tels que l’anxiété, et continuer à faire de l’exercice et à participer aux activités quotidiennes normales. Ce sont toutes des techniques importantes qui aident les patients à s’adapter à la vie avec la SEP. Il n’existe aucune preuve que les épisodes précipités de SEP, comme l’exercice, aggravent l’évolution à long terme de la maladie.
Pour soulager la douleur causée par la SEP, les patients tentent souvent de refroidir leurs extrémités chaudes et rouges avec de la glace ou de l’eau froide et utilisent continuellement des ventilateurs puissants à proximité des extrémités, mais ces actions peuvent augmenter le risque de lésions tissulaires, d’ulcérations et d’invalidité. .
L’eau et la glace peuvent entraîner une immersion du pied ou du pied de tranchée , avec gonflement et ulcération de la peau. Le vent peut également provoquer des blessures s’apparentant à des brûlures, avec exacerbation des bouffées de chaleur lorsque les ventilateurs sont arrêtés. Par conséquent, les mesures de refroidissement visant à soulager les symptômes doivent être sûres.
L’utilisation de glace ou d’immersion dans l’eau doit être évitée ou limitée (par exemple, 10 minutes et 4 fois/jour), et les patients doivent trouver d’autres moyens de refroidir leurs extrémités. Certains patients trouvent un soulagement en surélevant les extrémités pendant les symptômes. Les patients qui ont des épisodes de SEP après avoir fait de l’exercice, comme la course, peuvent être encouragés à essayer la natation.
| Traitements pharmacologiques |
La SEP est une maladie difficile à traiter. Des traitements topiques et systémiques peuvent être utilisés. Les résultats des traitements sont très variables. De nombreux rapports de traitement ont été décrits il y a plusieurs années (cette revue de la littérature couvre les années 1985-2021) ; Il existe peu de données publiées sur la durabilité des traitements rapportés.
Les médicaments topiques pour soulager l’érythème et la douleur peuvent être utilisés comme traitement de première intention et peuvent suffire à gérer cette maladie. Pour les patients atteints de SEP secondaire due à une maladie myéloproliférative, le traitement doit se concentrer sur la cause sous-jacente.
L’aspirine est le traitement systémique de première intention pour les patients atteints de SEP, en particulier ceux qui souffrent de maladies myéloprolifératives sous-jacentes . D’autres médicaments systémiques peuvent alors être envisagés.
L’application d’une approche d’équipe multidisciplinaire est bénéfique pour les soins aux patients atteints de SEP. Pour les patients atteints de SEP sévère, réfractaire ou handicapée, une orientation vers un centre complet de réadaptation contre la douleur est nécessaire.
| Traitements topiques |
Les traitements topiques sont considérés comme un traitement pharmacologique de première intention contre la SEP. Ils peuvent être efficaces pour supprimer la douleur ou les rougeurs (ou les deux), avec un besoin réduit de médicaments systémiques et moins d’effets indésirables par rapport aux médicaments systémiques.
De nombreux traitements topiques ont été utilisés pour traiter la SEP, avec différents niveaux d’efficacité. Certains traitements peuvent être utilisés principalement pour traiter la douleur associée à la SEP, tandis que d’autres peuvent diminuer les rougeurs et entraîner une diminution ultérieure de la douleur. Pour évaluer l’efficacité du médicament topique, il doit être utilisé pendant au moins 4 semaines avant de passer à un autre traitement.
> Thérapie topique de la douleur . Plusieurs médicaments topiques ont été utilisés : la lidocaïne, l’amitriptyline associée à la kétamine et la capsaïcine.
> Lidocaïne . Il s’agit d’un anesthésique local amide qui bloque les canaux sodiques nécessaires à l’initiation et à la conduction de l’impulsion neuronale, entraînant une anesthésie locale après application topique. Il peut être appliqué sous forme de crème, de pommade ou de patch sur les zones touchées (pieds, mains et autres zones). Les patchs de lidocaïne sont particulièrement pratiques pour être appliqués sur les surfaces dorsales ou plantaires du pied, où jusqu’à 3 patchs peuvent être utilisés pendant 12 à 24 heures. Les patchs peuvent être plus efficaces que la crème ou la pommade car la lidocaïne est administrée progressivement sur plusieurs heures. Dans une série de 34 patients atteints de SEP se présentant dans un centre tertiaire, la majorité ayant utilisé des patchs de lidocaïne à 5 % ont constaté une amélioration de la douleur, contrairement aux 10 patients qui n’ont pas répondu au gel de lidocaïne. Dans cette série, il a été observé que tous les patients avaient essayé plusieurs traitements avant le patch de lidocaïne et qu’en général, les patients présentant une maladie plus grave et plus longue avaient tendance à avoir une réponse plus faible qu’au patch de lidocaïne. Aucune absorption systémique de la lidocaïne ni aucun symptôme de toxicité de la lidocaïne n’ont été notés.
> Amitriptyline associée à la kétamine. Décrit pour la première fois pour une utilisation dans la SEP en 2006, cette combinaison topique dans un véhicule, appliquée sur les zones touchées jusqu’à 3 fois par jour, s’est avérée utile dans la gestion de la douleur liée à la SEP. L’amitriptyline, un antidépresseur tricyclique de première génération, inhibe la recapture de la sérotonine et de la noradrénaline et bloque les canaux sodiques nécessaires à l’initiation et à la conduction de l’impulsion neuronale.
La kétamine est un antagoniste du récepteur N-méthyl-D-aspartate dans les terminaisons périphériques des afférences nociceptives primaires ; par conséquent, il bloque également les impulsions neuronales et peut être efficace dans les ganglions de la racine dorsale et la corne dorsale. Dans une série de cas de 36 patients atteints de SEP, 75 % ont noté une amélioration de la douleur avec de l’amitriptyline topique à 1 à 2 % combinée à 0,5 % de kétamine. Si ce mélange de composés n’est pas efficace, la concentration en kétamine peut être augmentée, si nécessaire, jusqu’à 5 %. Cette combinaison doit être préparée comme une recette principale. En 2020, la FDA américaine a accordé la désignation de médicament orphelin à un gel topique d’amitriptyline (ATX01 ; AlgoTx) comme traitement de la SEP.
> Capsaïcine . La capsaïcine peut aider à contrôler la douleur cutanée grâce à la désensibilisation du récepteur TRPV1, entraînant une diminution de la libération de neurotransmetteurs tels que la substance P, un médiateur chimique important dans la transmission des impulsions douloureuses. Il existe peu de preuves étayant l’efficacité de la capsaïcine topique dans le traitement de la SEP. Un rapport de cas a noté que les symptômes de la SEP s’amélioraient avec l’application topique, 2 fois/jour, d’une crème de capsaïcine à 0,025 %. Deux enquêtes ont révélé que la capsaïcine n’était pas utile chez la plupart des patients. D’après notre propre expérience, la capsaïcine n’est généralement pas utile pour les patients atteints de SEP. Une crème ou une lotion topique à la capsaïcine (0,025 % à 0,075 %) peut être appliquée sur les zones touchées, 3 à 4 fois/jour pendant 6 semaines, et les patients doivent être avertis que le médicament peut provoquer des sensations initiales de picotement et de brûlure. Les patchs topiques de capsaïcine (0,025 %) peuvent être utilisés hors AMM sur les zones affectées car ils sont utilisés pour traiter la douleur neuropathique associée à la neuropathie périphérique diabétique des pieds ; jusqu’à 4 topiques en une seule application de 30 minutes, qui peut être répétée tous les 3 mois si nécessaire mais pas plus fréquemment. Théoriquement, les patchs de capsaïcine peuvent être utilisés à une dose plus élevée (8 %), désormais pour un usage clinique, pour le traitement de la douleur chronique ; Il peut être utile pour la prise en charge de la SEP, mais son utilisation dans ce trouble n’a pas été bien décrite.
> Autres traitements topiques . Les stratégies ne disposent que de preuves anecdotiques pour étayer leur utilisation. Par exemple, un mélange contenant jusqu’à 5 ingrédients peut être utilisé occasionnellement, en ajoutant des formulations topiques de ≥ 1 des éléments suivants au composé amitriptyline-kétamine : clonidine, gabapentine et lidocaïne. De manière anecdotique, les patchs transdermiques de clonidine (0,1 à 0,3 mg/jour) ont été utiles pour réduire la douleur liée à la SEP chez certains patients des auteurs. Ils offrent l’avantage d’être appliqués chaque semaine et, contrairement aux patchs de lidocaïne, peuvent être placés n’importe où sur le corps et pas nécessairement sur les zones touchées. La clonidine, un agoniste des récepteurs α2-adrénergiques, peut être utile dans le traitement de la SEP en diminuant l’écoulement sympathique central excessif à travers les récepteurs α2 et en neutralisant périphériquement la vasoconstriction aberrante.
D’autres traitements topiques possibles comprennent le gel de diclofénac à 1 % et la pommade à la gabapentine à 6 %. Les topiques en vente libre contenant du camphre ou du menthol associés à du salicylate de méthyle peuvent aider à combattre la douleur pendant les épisodes de SEP.
> Traitement topique de l’érythème. Les médicaments vasoactifs qui provoquent une vasoconstriction diminuent les rougeurs pendant les épisodes de SEP. Chez certains patients, cela se traduit par une diminution de la douleur. La midodrine, un agoniste α1, utilisé comme traitement topique, peut être utile. Dans une série de 12 patients, l’utilisation de midodrine à 0,2 % appliquée 3 fois/jour a amélioré les symptômes de la SEP, notamment les rougeurs.
D’autres médicaments topiques qui ne disposent que de preuves anecdotiques pour étayer leur efficacité peuvent être utiles pour réduire les rougeurs, tels que l’oxymétazoline topique à 0,05 % et le tartrate de brimonidine à 0,33 %, appliqués quotidiennement (approuvés par la FDA pour la rosacée) et le maléate de timolol à 0,5 %. Son utilisation continue peut provoquer un érythème dû à un effet rebond.
> Thérapie systémique. Considérations particulières . Si les traitements topiques seuls ne sont pas utiles, des traitements systémiques peuvent être utilisés. L’aspirine peut être utile et doit être essayée chez tous les patients qui ne présentent pas de contre-indications.
> Aspirine . Il est susceptible d’être efficace grâce à son mécanisme d’inhibition de la synthèse des prostaglandines et de l’agrégation plaquettaire. Il devrait être exploré comme traitement systémique de première intention contre la SEP, compte tenu de son faible coût et de son profil d’effets indésirables relativement faible. Pour les patients atteints de SEP qui n’ont aucune contre-indication à l’aspirine, une dose quotidienne de 325 mg est administrée pendant au moins 1 mois. L’aspirine est particulièrement efficace chez les patients atteints de SEP secondaire due à une maladie myéloproliférative sous-jacente, telle qu’une thrombocytose essentielle et une polyglobulie de Vaquez. Une amélioration spectaculaire a déjà été rapportée dès les premiers jours du traitement à l’aspirine. Les effets antiplaquettaires de l’aspirine la rendent particulièrement utile dans ce sous-groupe de patients. Dans une série de 57 cas, Davis et al. ont constaté que la moitié des patients ont signalé que l’aspirine avait amélioré leurs symptômes, bien que d’autres études basées sur des enquêtes n’aient trouvé aucune amélioration de la SEP. L’aspirine est le traitement initial le plus courant de la SEP en raison de sa sécurité globale, de son accessibilité et de son efficacité, en particulier chez les patients atteints de maladies myéloprolifératives.
> Autres médicaments non stéroïdiens. Pour les patients allergiques à l’aspirine, ces médicaments peuvent être utiles. Dans l’étude de Davis et al., près de la moitié des patients atteints de SEP ayant essayé l’ibuprofène, l’indométacine, la nabumetone, le naproxène ou le sulindac ont trouvé le traitement assez ou très utile. Le piroxicam a également été utilisé avec succès dans le traitement de la SEP primaire.
> Corticostéroïdes . Son administration systémique peut être indiquée dans un sous-groupe de patients atteints de SEP, au début de l’évolution de la maladie, avant l’apparition d’un éventuel remodelage nociceptif irréversible et d’une sensibilisation centrale. On pense que le mécanisme d’action des corticostéroïdes consiste à supprimer tout composant de la neuropathie inflammatoire. Bien que les mécanismes d’action exacts soient incertains, les corticostéroïdes peuvent fonctionner comme stabilisants membranaires. Une série rétrospective de 31 cas a identifié un sous-groupe sensible aux corticostéroïdes parmi ceux qui avaient un diagnostic déclencheur chirurgical, traumatique ou infectieux clair, et parmi ceux chez qui la maladie a atteint son intensité maximale en moins de 21 jours. Un essai avec des corticostéroïdes peut être justifié pour de nombreux patients atteints de SEP, quel que soit leur âge, en particulier au début de l’évolution de la maladie. Cependant, tous les patients ne répondent pas aux corticostéroïdes. Pour les patients atteints de SEP qui ont eu un début soudain ou aigu, un déclencheur clair ou une durée de moins d’un an, les auteurs recommandent un essai thérapeutique avec des corticostéroïdes systémiques pour évaluer leur efficacité. Un régime à dose très élevée peut être essayé. La dose recommandée est de 1 g/jour de méthylprednisolone par voie intraveineuse, pendant 3 jours consécutifs puis 1 fois/semaine pendant 11 semaines, ou de 1 g, 1 fois/semaine pendant 12 semaines. Après un essai de 12 semaines, l’amélioration subjective et objective du patient doit être évaluée. Si le patient présente des signes d’amélioration avec ce régime, l’utilisation d’agents immunosuppresseurs épargneurs de corticostéroïdes tels que l’azathioprine et le mycophénolate mofétil peut être envisagée, avec une diminution progressive des corticostéroïdes systémiques sur 3 à 6 mois. Pour un régime oral à forte dose, les auteurs recommandent une dose quotidienne d’au moins 40 mg de prednisone (ou équivalent corticostéroïde), 5 jours, pour un total d’au moins 200 mg de prednisone. Un régime à très haute dose peut être plus efficace qu’un régime à forte dose. Des recherches supplémentaires sont nécessaires pour explorer le dosage idéal.
> Bloqueurs des canaux sodiques. Ces médicaments ont été étudiés en tant que traitement potentiel et prometteur de la SEP, en particulier avec la découverte que la variante de séquence du gène SCN9A qui code pour la sous-unité α des canaux sodiques voltage-dépendants pourrait être essentielle dans la pathogenèse de la SEP. SEP héréditaire primaire (représentant seulement environ 5 % des cas). Parmi les affections douloureuses neuropathiques, la SEP est la seule dans laquelle la variante séquentielle a été identifiée comme provoquant la douleur associée à cette affection et sert donc de cible potentielle. La variante séquentielle, une variante à gain de fonction, amène les canaux sodiques neuronaux Nav1.7 à s’ouvrir plus facilement et à rester ouverts, ce qui entraîne une activation neuronale répétée et prolongée dans ces neurones sensoriels. Même avant la découverte du variant SCN9A, les inhibiteurs des canaux sodiques tels que la lidocaïne et la mexilétine avaient déjà été utilisés pour traiter la douleur associée à la SEP et la lidocaïne pourrait être efficace. La mexilétine, un antagoniste non sélectif des canaux sodiques, fonctionne également comme un antiarythmique de classe 1b. Le chlorhydrate de mexilétine diminue le taux d’augmentation du potentiel d’action (phase 0) en inhibant le courant d’afflux de sodium. Dans l’étude de Davis et al., 2 patients sur 5 atteints de SEP ont rapporté que la mexiletine était quelque peu utile, tandis que les 3 autres n’ont pas trouvé le traitement utile. Dans des études in vitro et in vivo plus récentes utilisant des modèles animaux, la mexilétine a normalisé les propriétés aberrantes des canaux Nav1.7 mutés. 25 rapports de cas ont été trouvés sur l’efficacité de la mexilétine orale dans le traitement primaire de la SEP, y compris dans les cas pédiatriques.
La carbamazépine, un autre agent oral doté de propriétés de blocage des canaux sodiques, aurait procuré un soulagement considérable de la douleur, en particulier dans les cas de SEP avec variantes V400M du gène SCN9A, tant dans les cas familiaux que de novo . Plus précisément, la carbamazépine normalise l’activation des cellules ganglionnaires de la racine dorsale qui expriment les canaux Nav1.7 et atténue l’hyperexcitabilité thermique de ces neurones sensoriels.
> Etudes expérimentales sur les bloqueurs des canaux sodiques . Un petit essai randomisé et contrôlé de validation de principe a révélé qu’un bloqueur oral des canaux sodiques ciblant le canal sodique Nav1.7 améliore les symptômes de douleur liés à la SEP médiés par SCN9A. Il existe plusieurs nouveaux antagonistes des canaux sodiques Nav1.7, notamment le TV-45070 topique (également connu sous les noms de XEN402 et XPF-002) et le PF-05089771 oral), qui pourraient constituer des traitements prometteurs pour la SEP primaire à l’avenir. , même si ces agents font l’objet d’essais et ne sont pas encore disponibles dans le commerce. Un bloqueur sélectif des canaux sodiques Nav1.7 a inversé pharmacologiquement le phénotype induit par les neurones sensoriels dérivés de cellules souches pluripotentes et a bloqué la perception de la douleur chez les patients atteints de SEP héréditaire.
> Perfusion de lidocaïne . Historiquement, les perfusions de lidocaïne ont été utilisées pour traiter les syndromes douloureux aigus. Des exemples de perfusions de lidocaïne pour le contrôle de la douleur aiguë liée à la SEP incluent l’utilisation chez un patient adulte et un patient pédiatrique, qui étaient tous deux également en transition vers la mexiletine. Les schémas de perfusion de lidocaïne varient et comprennent un schéma posologique en bolus basé sur le poids de 1 à 2 mg/kg, une dose en bolus fixe de 50 à 100 mg et une perfusion continue de 1 mg/kg/heure. . La sécurité des perfusions de lidocaïne n’est pas claire et les effets neurologiques (problèmes d’élocution et troubles de l’état mental) sont fréquents. Par conséquent, les perfusions intraveineuses de lidocaïne ne sont actuellement pas recommandées pour la SEP. La mexiletine est une alternative orale beaucoup plus sûre.
> Infusion de kétamine . Les perfusions de kétamine ont été utilisées pour traiter les syndromes douloureux chroniques à des doses sous-anesthésiques, avec l’avantage supplémentaire de réduire les besoins en opioïdes. Il a été décrit comme une option thérapeutique pour un patient pédiatrique atteint de SEP. La kétamine peut être utilisée comme traitement analgésique adjuvant pour la SEP. Certains centres de douleur proposent des perfusions contenant une combinaison de kétamine et de lidocaïne. Bien que certains pourraient envisager un essai sur la perfusion de kétamine, les preuves à l’appui sont limitées et son utilisation est controversée en raison de ses effets indésirables et du risque d’abus.
> Nitroprussiate de sodium . Des perfusions de nitroprussiate de sodium ont été utilisées dans un sous-groupe de patients atteints de SEP et d’hypertension concomitante. Le nitroprussiate de sodium interagit avec l’oxyhémoglobine pour produire de l’oxyde nitrique, ce qui conduit finalement à un relâchement des muscles lisses vasculaires et à une diminution de la pression artérielle. Plusieurs rapports de cas de patients pédiatriques atteints de SEP ont signalé une amélioration des symptômes. Cependant, dans une enquête menée par Cohen, les symptômes de la SEP se sont aggravés chez un patient adulte traité au nitroprussiate de sodium. Pendant qu’ils reçoivent cette perfusion, les patients doivent être étroitement surveillés. La dose est progressivement augmentée jusqu’à 2-4 mg/kg/minute. Les preuves sur l’utilisation du nitroprussiate de sodium sont limitées.
> Immunoglobuline intraveineuse . L’immunoglobuline intraveineuse a amélioré les symptômes chez 2 patients atteints de SEP secondaire et peut être envisagée chez les patients atteints de maladies auto-immunes. Les preuves de cette utilisation sont donc limitées.
> Antidépresseurs qui inhibent la recapture de la sérotonine et de la noradrénaline . Ces médicaments ont été utilisés dans le traitement de la SEP avec un succès variable. On pense qu’ils affectent le contrôle vasculaire et agissent sur les fibres sympathiques, inhibant la recapture neuronale de la sérotonine, de la noradrénaline et de la dopamine, et améliorant l’activité des neurotransmetteurs dans le système nerveux central (SNC). Parmi les médicaments de ce groupe, c’est le plus fréquemment utilisé. Dans une étude pilote portant sur 10 patients, la venlafaxine s’est révélée être un traitement relativement sûr et efficace contre la SEP primaire, avec une amélioration des symptômes après la première semaine de traitement. Une autre étude a également rapporté que 2 patients atteints de SEP sur 3 présentaient une réponse à la venlafaxine. La sertraline a également été utilisée et, dans une étude menée par des membres de l’Erythromelalgia Association (TEA), les symptômes se sont améliorés chez 6 patients sur 9 traités par la sertraline. Cependant, la fluoxétine, un autre inhibiteur sélectif du recaptage de la sérotonine, a induit la SEP chez 1 patient. Il existe peu de données disponibles sur l’utilisation de la duloxétine dans le traitement de la SEP.
> Amitriptyline. L’antidépresseur tricyclique amitriptyline inhibe également la recapture de la sérotonine et de la noradrénaline et bloque également les canaux sodiques. La formulation orale s’est avérée efficace dans le traitement de la SEP dans un rapport de cas. La formulation topique a été associée à de la kétamine.
> Anticonvulsivants.
Gabapentine et prégabaline . Ces deux médicaments ont été utilisés dans le traitement de la SEP avec un succès variable. Son utilisation est fréquente pour le traitement des douleurs neuropathiques, son effet se fait probablement par liaison aux canaux calciques voltage-dépendants. La gabapentine est structurellement liée au neurotransmetteur acide gamma-aminobutyrique. La gabapentine prévient l’allodynie et l’hyperalgésie dans les modèles animaux, mais le mécanisme n’est pas connu. Le schéma posologique conventionnel pour initier la gabapentine orale est de 300 mg 3 fois/jour, bien que d’autres schémas posologiques puissent être envisagés et les doses peuvent être augmentées progressivement pour obtenir l’effet souhaité. Dans l’enquête de Cohen, un total de 16 patients ont signalé une amélioration, mais aucun n’a connu de rémission. McGraw et Kosek ont également noté une amélioration chez 2 patients atteints de SEP traités à la gabapentine. Le médicament est relativement sûr ; l’effet indésirable le plus courant est la sédation. L’apparition fréquente d’œdèmes des membres inférieurs a également été rapportée et peut contrecarrer les bienfaits apportés par les médicaments topiques.
La prégabaline, un analogue de l’acide gamma-aminobutyrique, peut diminuer la douleur neuropathique en se liant aux canaux calciques voltage-dépendants dans les tissus du SNC. Deux cas ont été rapportés décrivant l’amélioration de la SEP avec la prégabaline. Dans l’un des rapports de cas, le patient avait déjà reçu un traitement d’essai à base de gabapentine sans amélioration et utilisait également un traitement topique.
> Prostaglandine et analogues . Ces médicaments ont été utiles dans la prise en charge de la SEP en raison de leurs propriétés vasodilatatrices qui diminuent le shunt artério-veineux microvasculaire associé à la SEP.
> Iloprost (administration intraveineuse). C’est un analogue synthétique de la prostacycline qui dilate les vaisseaux sanguins et inhibe l’activation plaquettaire. Dans une étude pilote randomisée, en double aveugle et en groupes parallèles, 8 patients recevant de l’iloprost par voie intraveineuse présentaient significativement moins de symptômes et moins de dysfonctionnement sympathique par rapport à 4 patients recevant un placebo. La prostaglandine E1 et l’iloprost, un analogue synthétique de la prostacycline, sont administrés par perfusions continues, les patients doivent donc être étroitement surveillés.
> Misoprostol (administration orale). Le misoprostol est un analogue oral de la prostaglandine synthétique E1. Dans une étude croisée en double aveugle par rapport au placebo, le misoprostol administré par voie orale (0,4 à 0,8 mg/jour) a amélioré les symptômes et diminué le shunt artério-veineux microvasculaire par rapport au placebo. L’effet bénéfique du misoprostol est probablement dû à la diminution du shunt artério-veineux microvasculaire au niveau de la peau affectée. En général, étant donné la difficulté d’obtenir la formulation intraveineuse d’iloprost aux États-Unis, l’administration orale doit être envisagée avant d’opter pour la perfusion.
> Bloqueurs des canaux calciques. Ils comprennent l’amlodipine, le diltiazem et la nifédipine, qui ont été utilisés dans le traitement de la SEP avec des réponses variables. Certains auteurs suggèrent que ces bloqueurs pourraient réduire l’hyperémie dans la SEP en inhibant les réponses vasculaires induites par les récepteurs α2-adrénergiques. Davis et al. ont rapporté que 85 % des 20 patients atteints de SEP ayant utilisé des vasodilatateurs (diltiazem, nifédipine et autres) n’ont obtenu aucun bénéfice. Dans une enquête sur les TSA, un seul patient a noté un bénéfice de la nifédipine, tandis que les autres ont présenté des effets indésirables intolérables (par exemple, diarrhée), mais 6 patients sur 8 atteints de SEP ont bénéficié du diltiazem, avec une quasi-rémission chez 1 patient. . En revanche, il y a eu des cas dans lesquels des inhibiteurs calciques ont induit la SEP. D’après l’expérience des auteurs, les inhibiteurs calciques peuvent aggraver la SEP tandis que leur arrêt entraîne la résolution des symptômes de la SEP chez plusieurs patients. Par conséquent, ils ne recommandent généralement pas son utilisation.
> Magnésium . Le magnésium, par voie orale et intraveineuse, a été utilisé dans le traitement de la SEP en raison de sa propriété de blocage des canaux calciques (et donc vasodilatatrice). Dans une enquête sur les TSA, 8 patients sur 13 traités avec de fortes doses de magnésium par voie orale (600 à 6 500 mg/jour) ont présenté une amélioration des symptômes tandis que chez 1 patient, les symptômes de la SEP se sont aggravés. L’auteur de ce rapport recommande de commencer le traitement par le magnésium à la dose quotidienne recommandée (350 mg/jour pour les femmes et 420 mg/jour pour les hommes) pour l’augmenter progressivement, en fonction de la tolérance, car avec des doses excessives, il existe une possibilité de troubles gastro-intestinaux. problèmes dus à une intolérance digestive, ainsi qu’à une faiblesse musculaire, des bouffées vasomotrices, une hypotension, une bradycardie, une vision floue et des effets cognitifs. Dans l’enquête TEA, 2 patients ont eu la diarrhée lorsque la dose a été augmentée. En général, les produits à base de magnésium liquides ou solubles en vente libre sont mieux tolérés que les comprimés. Le magnésium peut également être administré par voie intraveineuse toutes les 2 à 3 semaines, à la dose de 2 g en perfusion pendant 2 heures, mais les données décrivant la réponse objective à ce régime sont limitées.
> Antihistaminiques . Ils peuvent être utilisés mais ont généralement une valeur limitée dans la prise en charge de la SEP. Bien que la SEP ne semble pas être une maladie médiée par l’histamine, certains chercheurs pensent qu’une réaction locale chronique pourrait être en cause, justifiant son utilisation. Le cas d’un enfant atteint de SEP primaire dont l’amélioration s’est partiellement améliorée grâce au chlorhydrate de cétirizine oral a été rapporté. La cyproheptadine, un antihistaminique et un antagoniste de la sérotonine, s’est avérée efficace pour soulager les symptômes et la peau chaude chez 2 patients atteints de SEP primaire après qu’ils n’aient pas répondu à d’autres médicaments anti-inflammatoires non stéroïdiens, dont l’aspirine. Cependant, dans l’enquête de Cohen, aucun des trois patients n’a bénéficié de son administration. Le pizotifène, un autre antihistaminique ayant une activité antagoniste de la sérotonine, s’est révélé efficace dans le traitement de la SEP familiale. Dans l’enquête susmentionnée, 2 membres de la TEA sur 3 ont bénéficié d’un traitement antihistaminique. Cependant, dans une étude de Davis et al., une amélioration s’est produite chez moins d’un quart des 28 patients à qui on avait prescrit des antihistaminiques (chlorhydrate de cyproheptadine ou diphenhydramine, phénylpropanolamine, triméprazine ou cimétidine). De tous les antihistaminiques, la cyproheptadine et le pizotifène pourraient être les plus prometteurs en raison de leur propriété supplémentaire de bloquer la sérotonine au niveau des récepteurs de la sérotonine.
> Bêta-bloquants . Des données limitées soutiennent l’utilisation de bêtabloquants chez les patients atteints de SEP. Dans l’étude de Davis et al., la plupart des patients n’ont signalé aucun bénéfice de ces bloqueurs (aténolol, nadolol, chlorhydrate de propranolol ou timolol), mais des patients ont parfois signalé une réponse bénéfique. Leurs mécanismes d’action dans la SEP n’ont pas été établis, mais on pense qu’ils diminuent les effets membranaires de type anesthésique liés à la dose.
> Opioïdes . Bien que l’utilisation à court terme d’opioïdes puisse contribuer à diminuer la douleur associée à la SEP, les opioïdes ne sont pas considérés comme une option thérapeutique pour la SEP, compte tenu des risques élevés, du potentiel de dépendance et de la nécessité d’un traitement à long terme.
> Autres mandataires. Des rapports de cas ont soutenu l’utilisation de plusieurs agents contre la SEP, notamment l’ergotamine, le sulodexide, la pentoxifylline, le busulfan, l’hydroxyurée, la prazosine, le sulfate de quinine, la ranolazine, le carisoprodol et la pentazocine.
| perfusion péridurale |
La bupivacaïne et la ropivacaïne sont des anesthésiques locaux qui diminuent l’hyperexitabilité des fibres nociceptives. L’hyperexcitabilité et la douleur sont diminuées par l’inhibition réversible des canaux sodiques voltage-dépendants dans les fibres nociceptives des ganglions du trijumeau, des ganglions de la racine dorsale et des fibres sympathiques.
En interférant avec la conduction des fibres nociceptives, la perfusion péridurale de bupivacaïne ou de ropivacaïne peut procurer un soulagement immédiat de la douleur, mais elle est souvent temporaire. Bien que les anesthésiques locaux seuls puissent apporter des bénéfices aux patients atteints de SEP, des opioïdes tels que le fentanyl ou la morphine peuvent être ajoutés pour un effet analgésique supplémentaire.
Les rapports sur l’utilisation des perfusions péridurales sont rares. Certains patients ont signalé un soulagement plus long de la douleur. Sur 11 patients ayant reçu des perfusions péridurales pour le traitement de la SEP réfractaire, 7 ont connu une rémission complète ou ont pu poursuivre leurs activités quotidiennes avec une douleur minime.
Les 4 patients restants ont également signalé un soulagement considérable de la douleur, mais des interventions supplémentaires, telles qu’une deuxième perfusion péridurale et une pharmacothérapie, ont été nécessaires à long terme.
Après 30 mois de suivi, une deuxième perfusion péridurale de bupivacaïne a soulagé tous les symptômes chez 1 patient. Bien qu’une deuxième perfusion péridurale puisse être bénéfique, une intervention pharmacologique (par exemple, oxcarbazépine, prégabaline ou mexiletine) après la perfusion peut être tout aussi efficace. Par conséquent, avant une deuxième perfusion, la douleur résiduelle doit être contrôlée par un traitement pharmacologique. "Notre expérience", disent les auteurs, "est limitée aux perfusions péridurales pour la prise en charge de la SEP, mais nous n’avons pas observé de soulagement de la douleur à long terme comme cela a été décrit dans les rapports publiés."
| Sympathectomie |
La sympathectomie a été décrite dans différents rapports. Certains résultats ont été couronnés de succès, mais d’autres non.
| Des soins prodigués par une équipe multidisciplinaire |
Les patients bénéficient souvent d’une approche d’équipe multidisciplinaire comprenant la dermatologie, la neurologie, la médecine vasculaire et la médecine de la douleur. Une approche multidisciplinaire peut être particulièrement utile pour les patients atteints d’une maladie grave. Pour les patients atteints d’une maladie myéloproliférative sous-jacente, la collaboration avec un oncohématologue est précieuse pour gérer la maladie sous-jacente.
Chez les patients atteints de neuropathie à petites ou grosses fibres, l’intervention du neurologue est importante. Si les patients souffrent d’un syndrome de douleur chronique, l’implication d’une équipe anti-douleur et une approche de rééducation de la douleur peuvent être extrêmement utiles.
Les patients atteints de SEP présentent généralement un syndrome de douleur chronique avec sensibilisation centrale.
Les effets sur leur vie peuvent être dévastateurs, et ils peuvent s’isoler chez eux et adopter des comportements extrêmes pour éviter de précipiter des épisodes de SEP. Certains patients sont en fauteuil roulant et généralement handicapés. Pour les patients atteints de SEP réfractaire dont la vie a été gravement affectée par la SEP ou qui n’ont eu aucune réponse aux autres traitements, un programme multidisciplinaire de douleur et de réadaptation devrait être envisagé.
Les centres complets de réadaptation contre la douleur proposent une équipe composée de médecins, psychologues, ergothérapeutes et physiothérapeutes. Il existe plusieurs programmes de réadaptation contre la douleur. Selon les auteurs, « nous proposons un programme de traitement de jour de trois semaines comprenant de la physiothérapie et de l’ergothérapie. La physiothérapie est destinée au reconditionnement du corps et à l’augmentation de la tolérance aux activités.
Les problèmes fonctionnels et comportementaux liés aux morbidités concomitantes sont abordés. L’utilisation d’analgésiques, en particulier d’opiacés, peut être réduite ou interrompue. Les auteurs rapportent les résultats de ces programmes menés dans leur établissement, affirmant qu’ils « ont amélioré l’état physique et le fonctionnement émotionnel des patients atteints de SEP sévère et persistante ». Après avoir participé à un programme de réadaptation contre la douleur de trois semaines, un patient confiné dans un fauteuil roulant en raison de la SEP a pu marcher et reprendre un mode de vie actif, notamment jouer au golf régulièrement, un bénéfice qui a duré des années.
Recommandations finales
|















