Riepilogo La carie nella prima infanzia è una grave malattia orale che causa una carie aggressiva. In particolare, un’associazione sinergica tra un fungo, Candida albicans, e un batterio cariogeno, Streptococcus mutans, favorisce lo sviluppo di biofilm molto acidi e difficili da eliminare, aggravando il danno virulento. Queste interazioni sono in gran parte mediate dalle glicosiltransferasi (GtfB) che legano i mannani nella parete cellulare di C. albicans. Qui, presentiamo un approccio enzimatico per mirare alle interazioni GtfB-mannano in questo consorzio tra regni utilizzando eso- ed endoenzimi che degradano il mannano. Questi eso ed endoenzimi sono altamente efficaci nel ridurre la biomassa del biofilm senza uccidere i microrganismi, oltre ad alleviare la produzione di un ambiente a pH acido che porta alla carie dentale. Per corroborare questi risultati, presentiamo prove biofisiche utilizzando la microscopia a forza atomica a molecola singola, il taglio del biofilm e l’analisi della topografia della superficie dello smalto. I dati mostrano una drastica diminuzione delle forze leganti di GtfB a C. albicans (riduzione di circa 15 volte) dopo il trattamento enzimatico. Inoltre, l’attività enzimatica ha interrotto la stabilità meccanica del biofilm e ha ridotto significativamente la demineralizzazione dello smalto dei denti umani senza effetti citotossici sui cheratinociti gengivali. I nostri risultati rappresentano un progresso significativo verso un nuovo intervento terapeutico non biocida contro i biofilm batterici e fungini patogeni mirati alle interazioni di legame tra ligando e recettore tra regni. Importanza La formazione di biofilm è un fattore chiave di virulenza responsabile di varie malattie infettive. In particolare, è noto che le interazioni tra un fungo, Candida albicans, e un batterio, Streptococcus mutans, svolgono un ruolo importante nella patogenesi della carie dentale. Sebbene alcuni antimicrobici siano stati applicati per trattare le malattie associate ai biofilm coinvolti nei funghi, questi spesso mancano di interazioni polimicrobiche mirate. Inoltre, questi potrebbero non essere appropriati per misure preventive perché questi antimicrobici possono alterare il microbiota ecologico e/o indurre la prevalenza della resistenza ai farmaci nel tempo. Prendendo di mira in modo specifico il meccanismo di interazione mediante il quale le mannoproteine sulla superficie di C. albicans mediano l’interazione tra regni, dimostriamo che gli enzimi che degradano le mannoproteine possono interrompere efficacemente le interazioni del biofilm senza effetti microbicidi o senza causare citotossicità nelle cellule. cellule umane. Ciò suggerisce una potenziale applicazione come approccio mirato per intervenire in un biofilm patogeno associato a una malattia orale costosa e irrisolta. |
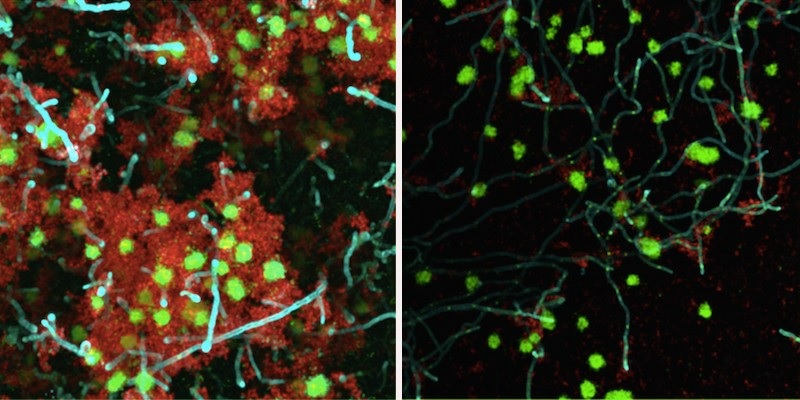
Un trattamento enzimatico ha indebolito significativamente un biofilm di batteri e lieviti su una superficie simile a un dente. Questo approccio terapeutico, che utilizza la beta-mannanasi (pannello di destra) per rompere i legami tra batteri e lieviti, potrebbe essere utilizzato per trattare la carie della prima infanzia, una forma grave di carie. (Immagine: per gentile concessione di Geelsu Hwang)
Commenti
Prendendo di mira i collegamenti tra batteri e lieviti che possono formare la placca dentale, una nuova strategia terapeutica potrebbe aiutare a eliminare l’accumulo senza intaccare i tessuti orali, secondo un nuovo studio condotto da un team dell’Università della Pennsylvania.
La combinazione di una dieta ricca di carboidrati e di una scarsa igiene orale può lasciare i bambini affetti da carie nella prima infanzia (ECC), una grave forma di carie che può avere un impatto duraturo sulla loro salute orale e generale.
Alcuni anni fa, gli scienziati della Penn’s School of Dental Medicine hanno scoperto che la placca dentale che dà origine al CPB è composta sia da una specie batterica, Streptococcus mutans , sia da un fungo, Candida albicans . I due formano una simbiosi appiccicosa, conosciuta scientificamente come biofilm, che diventa estremamente virulento e difficile da rimuovere dalla superficie del dente.
Ora, un nuovo studio del gruppo offre una strategia per distruggere questo biofilm prendendo di mira le interazioni lievito-batteri che rendono le placche ECC così intrattabili. A differenza di alcuni attuali trattamenti per il CPB, che utilizzano agenti antimicrobici che possono avere effetti indesiderati e potenzialmente danneggiare i tessuti sani, questo trattamento utilizza un enzima specifico per i legami esistenti tra i microbi.
"Abbiamo pensato che questo potesse essere un nuovo modo per affrontare il problema della CEC che sarebbe intervenuto nell’interazione sinergica tra batteri e lieviti", afferma Geelsu Hwang, assistente professore alla Penn Dental Medicine e autore senior dello studio, pubblicato sulla rivista. mBio. "Questo ci dà un altro strumento per distruggere questo biofilm virulento."
Il lavoro si basa sui risultati di un articolo del 2017 di Hwang e colleghi, tra cui Hyun (Michel) Koo della Penn Dental Medicine, che ha scoperto che le molecole chiamate mannani nella parete cellulare della Candida si legano strettamente a un enzima secreto da S. mutans, le glicosiltransferasi ( Gftb). ). Oltre a facilitare il legame tra regni, Gftb contribuisce anche alla tenacia dei biofilm dentali producendo polimeri simili a colla chiamati glucani in presenza di zuccheri.
Sebbene alcuni casi di ECC siano trattati con farmaci che uccidono direttamente i microbi, riducendo potenzialmente il numero di agenti patogeni nella bocca, ciò non sempre distrugge efficacemente il biofilm e può avere effetti indesiderati sui microbi "buoni" e sui tessuti molli. della cavità orale.
Hwang e i suoi colleghi volevano provare un approccio diverso che mirasse direttamente all’insidiosa interazione tra lievito e batteri e hanno scelto di prendere di mira i mannani sulla superficie della cellula di Candida come punto di contatto.
Utilizzando tre diversi enzimi che degradano il mannano , ne hanno applicato ciascuno un biofilm che cresceva su una superficie simile a un dente in un mezzo di saliva umana e lo hanno lasciato per cinque minuti. Dopo il trattamento, hanno notato che il volume totale del biofilm era ridotto. Usando una potente microscopia, hanno anche osservato riduzioni drammatiche dello spessore del biofilm e delle interazioni tra batteri e lieviti. Il pH del mezzo circostante era più alto quando esposto agli enzimi, indicando un ambiente non altrettanto acido e quindi meno favorevole alla carie.
Hanno anche misurato quanto fosse facile abbattere il biofilm dopo il trattamento, utilizzando un dispositivo che applica una tensione, simile a quando si lava i denti.
"La struttura del biofilm era più fragile dopo il trattamento enzimatico", afferma Hwang. "Abbiamo potuto vedere che i biofilm venivano rimossi più facilmente."
Per confermare il meccanismo del loro approccio, ovvero che gli enzimi che degradano il mannano indebolivano il legame tra lievito e batteri, il team ha utilizzato la microscopia a forza atomica per misurare i legami tra Candida e Gftb. Hanno scoperto che la terapia riduceva la forza di questo legame di 15 volte.
Infine, volevano avere un’idea di quanto sarebbero stati ben tollerati questi enzimi se utilizzati nella cavità orale, soprattutto perché i bambini sarebbero il gruppo di pazienti target.
Quando hanno applicato gli enzimi alle cellule gengivali umane in coltura, non hanno riscontrato alcun impatto dannoso, anche quando hanno utilizzato una forma concentrata degli enzimi. Inoltre, hanno osservato che il trattamento non uccide batteri o lieviti, segno che potrebbe funzionare anche se i microbi sviluppassero mutazioni che conferirebbero loro resistenza contro altri tipi di terapie.
I ricercatori hanno mantenuto il tempo di applicazione relativamente breve a cinque minuti, anche se si aspettano di vedere l’attività in un tempo ancora più breve, come i due minuti consigliati per lavarsi i denti. Hwang dice che si potrebbe prendere in considerazione un collutorio senza alcool con questi enzimi aggiunti che i bambini potrebbero usare come misura preventiva contro la malattia coronarica.
I ricercatori sperano di continuare a perseguire questa possibilità con ulteriori follow-up, incluso il test di questi enzimi in un modello animale. Con ulteriori successi, mirano ad aggiungere un altro strumento per combattere la minaccia per la salute pubblica rappresentata dalle malattie coronariche.
















