1. Il virus
SARS-CoV-2 contiene più di 30.000 basi di RNA. Un meccanismo di correzione di bozze impedisce a questo grande genoma di accumulare frequenti mutazioni. La grande proteina spike (S) forma una sorta di corona sulla superficie delle particelle virali. Il suo dominio di legame con il recettore interagisce con alta affinità con i recettori dell’enzima di conversione dell’angiotensina 2 (ACE2) sulla superficie delle cellule ospiti.
Dopo l’attaccamento, due proteasi della cellula ospite (Furin e TMPRLRS) scindono le proteine spike e i loro peptidi di fusione esposti fondono la membrana del virus con la membrana della cellula ospite. L’RNA del virus entra nelle cellule del tratto respiratorio superiore e inferiore e viene tradotto in proteine virali. Altri punti di ingresso sono sotto indagine. La cellula muore , rilasciando milioni di nuovi virus che infettano altre cellule e altri individui[1].
2. L’infezione
Esistono diversi modi in cui la SARS-CoV-2 si diffonde. L’infezione inizia con la competizione tra i virioni SARS-CoV-2 che hanno raggiunto la mucosa respiratoria che esprime alti livelli di recettori ACE2 e la barriera creata dal muco secreto dalle cellule caliciformi e mosso da ciglia simili a capelli e reazioni immunitarie. innato.
Esistono prove della presenza del virus in cellule diverse dall’epitelio respiratorio, comprese le cellule epiteliali gastrointestinali, le cellule endoteliali e le cellule mieloidi. Non sappiamo ancora quanti SARS-CoV-2 vengono eliminati; Tuttavia, l’efficacia delle prime risposte di difesa determina se l’infezione sarà benigna o avrà conseguenze gravi.
La Figura 1 mostra i determinanti selettivi della suscettibilità al COVID-19, tra cui la carica virale, l’invecchiamento, lo stile di vita e possibilmente la genetica. Se i virioni SARS-CoV-2 iniziano a replicarsi, possono raggiungere e distruggere le cellule negli alveoli polmonari e nel tratto gastrointestinale. Una reazione eccessiva immunitaria ( tempesta di citochine ) può aumentare il danno tissutale [2, 3] Figura 1: Una rappresentazione schematica della patogenesi di COVID-19. ACE2, enzima di conversione dell’angiotensina 2, recettori Toll-TLR, M? macrofagi, cellule dendritiche DC, interferone IFN, interferone freccia basso IFN basso, sindrome da distress respiratorio acuto ARDS, i punti indicano che sono coinvolti più recettori (ad esempio CD147 per l’ingresso virale).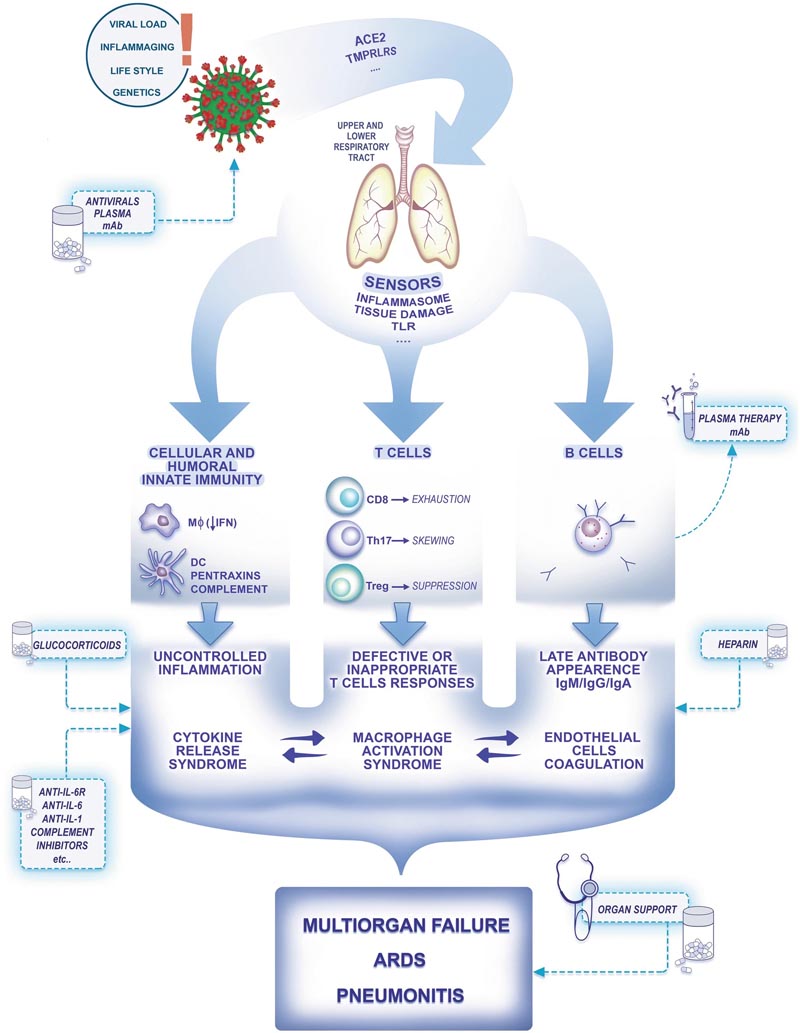
3. Immunità
L’immunità cellulare e umorale innata rappresentano una prima linea di resistenza responsabile della maggior parte degli incontri con agenti infettivi. Le prove della SARS-CoV-1 suggeriscono che questi virus possono bloccare l’immunità antivirale mediata dall’interferone (Fig. 1). Le cellule T citotossiche CD8 svolgono un ruolo critico nella resistenza antivirale.
Le prove suggeriscono che durante il COVID19 le cellule T sperimentano un esaurimento funzionale con linfopenia , orientandosi verso un fenotipo Th17, inappropriato per l’immunità e la soppressione antivirale (Fig. 1) [4]. La produzione di anticorpi avviene tardi dopo l’esposizione (fino a 20 giorni) e dopo la comparsa dei sintomi (fino a 15 giorni per il 100% dei pazienti con punteggio positivo) [5] .
È interessante notare che gli anticorpi IgA sono presenti nel sangue e nella saliva e possono svolgere un ruolo chiave nell’immunità. Esistono prove che i casi sintomatici di COVID-19 causano memoria immunologica e resistenza alla reinfezione . Secondo la SARS, la memoria immunologica può durare dai 2 ai 3 anni , un aspetto chiave dell’immunità che deve essere definito.
4. Infiammazione
L’infiammazione svolge un ruolo chiave nello sviluppo di COVID-19 dall’infezione da SARS-CoV-2. I sensori dell’infezione virale e del danno cellulare (p. es., inflammasomi; TLR) attivano la produzione dipendente dalle cellule mieloidi di citochine infiammatorie (p. es., IL-1; IL-6; chemochine). I macrofagi e le citochine infiammatorie amplificano l’infiammazione locale e sistemica e sono i principali fattori di insufficienza d’organo (Fig. 1).
Sebbene il ruolo dell’infiammazione nel COVID-19 sia ovvio, non è chiaro se la modulazione della risposta infiammatoria con i farmaci possa apportare benefici. Attualmente sono allo studio diversi farmaci.
5. Trombosi
Come previsto per una malattia caratterizzata da uno stato infiammatorio in risposta ad un’infezione virale, le complicanze tromboemboliche venose e arteriose sono comuni nei pazienti ospedalizzati [6] . Nei polmoni sono presenti microtrombi e le alterazioni della cascata della coagulazione possono essere misurate a livello sistemico. La disfunzione endoteliale causata sia dall’effetto citopatico diretto del virus che dalla reazione infiammatoria porta ad un ambiente pro-trombotico [3, 7].
Nei pazienti ospedalizzati, dovrebbe esserci una soglia bassa per rilevare complicanze tromboemboliche. D’altra parte, sono necessarie ulteriori ricerche per esaminare il ruolo dei regimi anticoagulanti rispetto alla tromboprofilassi standard nel trattamento di questi pazienti [8].
6. Test diagnostici
La pietra angolare dei test diagnostici è attualmente la valutazione dell’RNA virale nei campioni di lavaggio nasale o broncoalveolare mediante RT-PCR. La RT-PCR con tampone rappresenta un collo di bottiglia e si spera che i test basati sulla saliva possano rispondere all’urgente necessità di test diffusi.
Sono stati sviluppati più di 100 test sierologici nell’industria o nelle istituzioni accademiche, molti dei quali scarsamente caratterizzati. Considerati i tempi e le caratteristiche della risposta anticorpale, test adeguatamente validati sono essenziali per gli studi epidemiologici, la valutazione delle donazioni di plasma, la valutazione della memoria e della risposta al vaccino e come diagnostica complementare nei pazienti negativi alla RT-PCR.
Non ci sono dati disponibili per dimostrare che un certo livello di anticorpi sia associato alla protezione contro la successiva esposizione a SARS-CoV-2. Pertanto non vi è alcuna ragione per "passaporti di immunità" o "licenze di immunità" . Una falsa percezione di essere “immuni” può incoraggiare comportamenti irresponsabili [9] .
7. Aspetti clinici
L’infezione da SARS-CoV-2 presenta una varietà di sintomi: può essere completamente asintomatica o presentarsi con sintomi gravi. Il periodo di incubazione del SARS-CoV-2 è di 5,1 (4,5-5,8) giorni [10] . La prevalenza della disfunzione d’organo varia. L’ARDS è stata segnalata da un minimo del 3,4% a oltre il 10% dei casi positivi [3, 11, 12].
In Italia, mentre il Paese ha registrato la più alta incidenza giornaliera di nuovi casi, circa il 67% dei pazienti ha mostrato sintomi lievi e circa il 30% ha avuto sintomi che hanno richiesto il ricovero ospedaliero. I sintomi più comuni sono febbre e tosse . Una piccola percentuale di casi riferisce sintomi gastrointestinali prima della comparsa dei sintomi respiratori.
I pazienti più anziani con comorbidità hanno maggiori probabilità di essere gravemente colpiti e di morire. La ragione più comune per il ricovero in terapia intensiva è l’insufficienza respiratoria acuta . Molti pazienti hanno sviluppato ARDS grave. Spesso è presente il coinvolgimento di altri organi.
8. Terapia
I pilastri del trattamento sono la terapia di supporto, il supporto respiratorio e la gestione dell’insufficienza d’organo. Attualmente non esiste un trattamento specifico per la SARS-CoV-2 [13] . La clorochina e l’idrossiclorochina sono state ampiamente utilizzate; Tuttavia, stanno emergendo sempre più prove sulla sua mancanza di efficacia e sui possibili danni .
Gli studi stanno attualmente valutando il ruolo degli antivirali, degli steroidi e delle terapie immunomodulanti . Prove emergenti sull’elevata incidenza di complicanze tromboemboliche arteriose e venose stanno attribuindo all’eparina un potenziale ruolo nella prevenzione di questi eventi.
Il plasma di pazienti guariti è stato utilizzato in Cina e altrove, inclusa l’Italia, come fonte di anticorpi, come è stato fatto per la SARS e la MERS. La sua sicurezza ed efficacia in questa malattia sono state attualmente studiate.
9. Vaccini anti-SARS-CoV-2
Poiché non sappiamo ancora se la protezione contro il COVID-19 si basi sull’azione degli anticorpi o sull’attività delle cellule T, l’attuazione di circa 150 programmi per lo sviluppo di vaccini basati su diverse piattaforme tecnologiche è pienamente giustificata [14].
Per verificare l’efficacia del vaccino in base alle “regole sull’uso di emergenza” , è stato proposto di vaccinare volontari umani e poi sfidarli intenzionalmente. L’OMS propone di dare priorità all’efficacia dei vaccini più promettenti in studi coordinati. Inizialmente, potrebbe non essere fisicamente possibile produrre abbastanza vaccini per la popolazione mondiale. Tuttavia, l’OMS sta cercando di garantire che siano condivisi equamente, una sfida cruciale.
10. Preparazione e ulteriori ricerche
Se una cosa è evidente dai tanti morti di questa pandemia, è che il mondo non era preparato dal punto di vista strutturale, politico, clinico e di ricerca.
Diversi operatori sanitari hanno perso la vita. Si tratta di una perdita molto grave che nessun paese può permettersi di ripetere.
I due principi chiave che devono essere seguiti per controllare un potenziale aumento di pazienti malati sono aumentare la capacità di aumento e, cosa ancora più importante, contenere la trasmissione comunitaria del virus .
Durante un cluster non controllato, il volume di pazienti che necessitano di ricovero in terapia intensiva può essere molto elevato e dovrebbero essere compiuti sforzi per aumentare garantendo al tempo stesso la sicurezza dei pazienti e degli operatori sanitari non-COVID-19 [15, 16].
Un’ampia gamma di approcci terapeutici sono stati testati in condizioni non controllate. Oggi, come mai prima d’ora, abbiamo un disperato bisogno di recuperare i concetti di medicina di precisione che hanno impiegato decenni per svilupparsi.
Dobbiamo continuare i nostri sforzi per fornire il trattamento giusto al paziente giusto al momento giusto. Non dovremmo cercare la “pistola magica ”, ma dovremmo lodare gli sforzi per rispondere alle domande della ricerca, e se la risposta porta nuove domande, dovremmo lodarle ancora di più.
Lo studio WHO SOLIDARITY o REMAP-CAP, uno studio progettato in modo adattivo, è un modo promettente per rispondere ad alcune di queste domande di ricerca [17].
Foto di Javier Matheu su Unsplash