Points forts Dans cette étude, les auteurs ont utilisé une méthode Delphi modifiée pour obtenir un consensus d’experts sur la définition et les catégories de gravité de l’exacerbation de la maladie pulmonaire obstructive chronique (MPOC). Le groupe d’experts a proposé d’incorporer des valeurs cliniques et de laboratoire mesurables, notamment la gravité de la dyspnée, la saturation en oxygène, la fréquence respiratoire, la fréquence cardiaque, la protéine C-réactive et les gaz du sang artériel. Cette définition mise à jour, appelée « proposition de Rome » , contribuera à standardiser la prise en charge des patients diagnostiqués avec une exacerbation aiguë de la BPCO et à homogénéiser la recherche. |
Où nous sommes?
Connaissances scientifiques sur le sujet :
Des définitions précises et pratiques des événements médicaux aigus sont nécessaires si les médecins veulent diagnostiquer et traiter efficacement les patients, fournir des informations pronostiques et mettre en œuvre une médecine de précision. La définition actuelle de l’exacerbation de la maladie pulmonaire obstructive chronique (MPOC) est subjective et basée uniquement sur l’aggravation des symptômes respiratoires. De plus, la gravité est classée post hoc par la ressource de soins de santé utilisée pour traiter l’événement. Ces lacunes justifient la nécessité de réviser la définition de l’ECOPD.
Ce que cette étude ajoute au domaine :
La proposition de Rome pour une définition actualisée de l’ECOPD comble bon nombre des lacunes des définitions plus anciennes. Basé sur une revue approfondie de la littérature et utilisant la méthodologie Delphi, il précise la période de temps au cours de laquelle l’aggravation des symptômes définit une ECOPD.
Deuxièmement, à l’aggravation subjective des symptômes, elle ajoute une série de variables cliniques objectivement mesurables et facilement disponibles : dyspnée, saturation en oxygène, fréquence respiratoire, fréquence cardiaque, protéine C-réactive et, si nécessaire, gaz du sang artériel.
Troisièmement, sur la base de seuils convenus, il intègre ces variables dans trois catégories de gravité mutuellement exclusives qui peuvent être utilisées pour classer la gravité de l’exacerbation lors du premier contact avec le patient. Cette proposition vise à faciliter et à améliorer les soins cliniques, la recherche et la planification des services de santé.
La définition actuelle de l’exacerbation de la maladie pulmonaire obstructive chronique (MPOC) repose uniquement sur l’aggravation des symptômes respiratoires, avec une gravité classée a posteriori par la ressource de soins utilisée pour traiter l’événement, qui peut varier selon les professionnels et les systèmes. sanitaire.
Ces lacunes justifient la nécessité de réviser la définition de l’ECOPD et la classification de la gravité pour en faire une définition utile au moment du contact avec le patient. Pour y parvenir, un groupe d’experts a utilisé une méthode Delphi modifiée composée de cinq séries de questions générées par une revue complète de la littérature, complétée par des discussions virtuelles. Pour les 80 questions identifiées, le niveau d’accord a été évalué à l’aide d’une échelle de Likert allant de 0 (fortement en désaccord) à 9 (fortement d’accord). Le consensus était défini a priori par un score médian ≥7 (accord fort).
Le modèle conceptuel ECOPD et la définition proposée
Les preuves actuelles indiquent qu’une ECOPD est caractérisée par une explosion aiguë d’inflammation des voies respiratoires due à des bactéries, des virus, des polluants environnementaux ou d’autres stimuli (Figure 1). Cela a été documenté par des études soigneusement menées en milieu ambulatoire et hospitalier, de nombreuses études montrant que le processus inflammatoire peut se propager de manière systémique.
Cette poussée inflammatoire, ainsi que l’aggravation de la limitation existante du débit d’air, augmentent le travail respiratoire chez les patients ayant une réserve respiratoire limitée.
Un cercle vicieux d’augmentation de la résistance des voies respiratoires et de tachypnée entraîne un piégeage de gaz dans les poumons, un dysfonctionnement des muscles respiratoires, une aggravation de la dyspnée et une inadéquation ventilation-perfusion se manifestant par une hypoxémie artérielle avec ou sans hypercapnie . Chez certains patients, la demande ventilatoire dépasse la réserve, entraînant une insuffisance ventilatoire, une hypercapnie et une acidose respiratoire qui, si elles ne sont pas traitées, peuvent entraîner la mort.
Méthode de diagnostic
1) Ces événements peuvent mettre la vie en danger et nécessiter une évaluation et un traitement appropriés.
2) Effectuer une évaluation clinique approfondie pour détecter les signes de BPCO et d’éventuelles comorbidités respiratoires et non respiratoires, y compris la prise en compte des causes alternatives des symptômes et des signes du patient ; principalement la pneumonie, l’insuffisance cardiaque et l’embolie pulmonaire.
3) Évaluer :
a) Symptômes ; gravité de la dyspnée à l’aide de l’EVA et documentation de la présence de toux.
b) Signes (tachypnée, tachycardie), volume et couleur des crachats et difficultés respiratoires (utilisation des muscles accessoires).
4) Évaluer la gravité par des examens supplémentaires appropriés tels que : oxymétrie de pouls, évaluation en laboratoire, CRP et/ou gaz du sang artériel.
5) Établir la cause de l’événement (virus, bactérien, environnemental, autre).
Causes, mécanismes pathobiologiques et conséquences physiopathologiques d’une exacerbation de BPCO
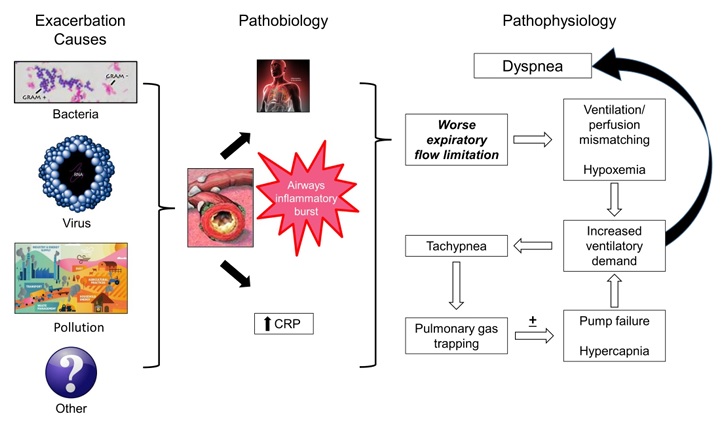
BPCO, maladie pulmonaire obstructive chronique ; EVA, échelle visuelle analogique ; CRP, protéine C-réactive.
Définitions
| La définition proposée stipule : « Chez un patient atteint de BPCO, une exacerbation est un événement caractérisé par une dyspnée et/ou une toux et des crachats qui s’aggravent en ≤ 14 jours, pouvant s’accompagner d’une tachypnée et/ou d’une tachycardie, souvent associées à une augmentation locale et inflammation systémique causée par une infection des voies respiratoires, la pollution ou d’autres dommages aux voies respiratoires. |
Classification de la gravité de l’EPOCD
La classification actuelle de la gravité de l’ECOPD, basée sur l’utilisation post-facto des ressources de santé, constitue une limitation majeure de la définition actuelle. En raison de la variabilité mondiale des ressources disponibles pour traiter les patients et des coutumes locales qui affectent les critères de visites et d’admissions à l’hôpital, il existe une variabilité substantielle dans les résultats rapportés par l’ECOPD. Ceci est particulièrement important pour interpréter les résultats des études d’intervention et pour planifier de futurs essais cliniques.
Trois catégories de sévérité (légère, modérée ou sévère) ont été définies en intégrant six variables cliniquement mesurables :
- Intensité de la dyspnée
- Saturation d’oxygène
- Fréquence respiratoire
- Rythme cardiaque
- Protéine C-réactive
- Si indiqué, gaz du sang artériel.
Ces variables ont été convenues par consensus à partir d’une liste possible de 21 qui ont fait l’objet d’une revue exhaustive de la littérature et d’une discussion. Parmi ces variables possibles, l’aggravation de la toux et des crachats méritait une attention particulière. Au cours de l’ECOPD, une toux et une augmentation des crachats ou un changement de couleur peuvent survenir et, dans une proportion de cas, cela peut être le symptôme ou le signe le plus pertinent ; cependant, son intensité n’a pas été correctement mesurée, ce qui rend difficile son inclusion dans la classification de gravité de l’ECOPD.
Cependant, bien que la toux et les crachats restent une partie intégrante de la définition de l’ECOPD, les panélistes ont convenu que l’aggravation de la dyspnée est le symptôme le plus pertinent pour la plupart des patients et, puisqu’il est mesurable, il est utile de classer la gravité de l’épisode.
Hypoxémie et hypercapnie
Le déséquilibre ventilation-perfusion (VA/Q) est le mécanisme le plus important responsable des anomalies des échanges gazeux dans la BPCO.
Étant donné qu’une BPCO stable peut être associée à une hypoxémie artérielle avec ou sans hypercapnie, des mesures absolues et un changement de valeurs seraient utiles comme déterminants de la gravité. L’évaluation des gaz du sang est idéale mais n’est pas disponible dans tous les contextes cliniques, tandis que l’oxymétrie de pouls est pratique et largement disponible, même si nous reconnaissons qu’elle peut être moins précise chez les patients noirs.
L’insuffisance respiratoire hypercapnique décompensée est connue pour être associée à une mortalité accrue qui est réduite par la ventilation non invasive (VNI). Bien que les sociétés d’experts recommandent de titrer l’oxygène supplémentaire pendant l’ECOPD jusqu’à une SaO2 de 88 à 92 % (7, 55), les études de l’ECOPD suggèrent que la réduction moyenne de la SaO2 n’était pas supérieure à 2 %.
Sur la base de ces preuves, le panel a convenu que lorsque le changement par rapport à la valeur initiale est connu, une ECOPD légère serait caractérisée par une saturation artérielle en oxygène (SaO2) ≥92 % et un changement ≤3 %, un événement modéré serait une SaO2 <92 % et /ou une variation > 3 %, et un événement sévère dû à une insuffisance respiratoire hypercapnique acidotique , c’est-à-dire pression partielle artérielle de dioxyde de carbone (PaCO2) > 45 mmHg et pH < 7,35.
Protéine C-réactive sérique
Une valeur de CRP ≥ 10 mg/L peut aider à distinguer les ECOPD légères des modérées.
Les sujets sains, les fumeurs sans BPCO et les patients atteints de BPCO stable ont généralement des valeurs de CRP <10 mg/L, des valeurs plus élevées dans cette plage étant associées à un risque accru d’hospitalisation et de décès. Les taux sériques de CRP augmentent dans les ECOPD virales et bactériennes, bien qu’ils soient généralement plus élevés dans ces derniers, de sorte que les valeurs au point d’intervention peuvent être utilisées pour guider l’antibiothérapie.
Chez les patients ambulatoires atteints de BPCO et d’ECOPD, les taux de CRP augmentent légèrement par rapport aux valeurs de base. Chez les patients aux urgences ou admis à l’hôpital, des valeurs de CRP plus élevées ont été rapportées, comprises entre 8 et 156 mg/L.
Bien que le panel ait reconnu le manque de spécificité de la CRP sérique en tant que marqueur de l’inflammation des voies respiratoires ou des poumons, un consensus a été atteint sur le fait qu’une valeur de CRP ≥ 10 mg/L peut aider à distinguer les ECOPD légères des modérées. .
Nous n’avons pas attribué à la CRP un poids différent de la FC, de la RR ou de la saturation en oxygène. Un patient pourrait avoir un épisode plus sévère défini exclusivement par une combinaison de signes cliniques sans CRP > 10 mg/L. Notre proposition vise à contribuer à l’inclusion d’au moins un marqueur mesurable au point d’intervention, dont le seuil peut être modifié au fil du temps, si cette proposition est mise en œuvre et que les résultats le suggèrent.
Intégration de variables dans une échelle pratique d’évaluation de la gravité
Les panélistes ont convenu que l’intégration de cinq paramètres faciles à évaluer (dyspnée, fréquence respiratoire, fréquence cardiaque, saturation en oxygène et CRP sérique) sera utilisée pour évaluer la gravité d’une ECOPD, à la fois dans l’évaluation clinique des patients et dans recherche. et les essais cliniques.
|
La proposition de Rome pour une définition actualisée et une classification de la gravité de l’ECOPD a été rédigée par un groupe international d’experts, en utilisant un cadre axé sur la faisabilité et la validité potentielle. Un consensus a été atteint en utilisant une méthodologie Delphi modifiée, basée sur les données d’études rapportant des mesures objectives des symptômes, des signes, des variables physiologiques et des biomarqueurs.
La valeur prédictive des variables classifiant la gravité a été évaluée en utilisant l’intensité potentielle des soins nécessaires au traitement et à la stabilisation du patient. Cette définition révisée comble bon nombre des lacunes de la définition actuelle et devrait mieux éclairer la planification des soins cliniques, de la recherche et des services de santé, mais doit être validée de manière prospective dans des études correctement conçues et alimentées.
Autres tests importants
Les panélistes ont examiné 16 autres tests cliniques et de laboratoire utilisés dans le diagnostic et la classification de la gravité de l’ECOPD. Parmi ceux-ci, plusieurs appellent quelques commentaires.
La spirométrie de routine ou toute évaluation de la fonction pulmonaire ne peut pas être obtenue de manière fiable au cours d’une ECOPD, car les patients sont généralement trop malades pour effectuer une manœuvre de spirométrie adéquate, les changements par rapport aux valeurs initiales sont souvent faibles et les résultats antérieurs à l’ECOPD peuvent ne pas être disponibles.
Les panélistes pensaient également que les efforts déployés pour développer des dispositifs précis pouvant aider à surveiller la fonction pulmonaire au fil du temps constitueraient une avancée importante dans notre capacité à intégrer cette variable dans les améliorations futures de cette proposition.
Les éosinophiles du sang périphérique pourraient être utilisés comme guide thérapeutique, en particulier en ce qui concerne l’utilisation systémique de stéroïdes, mais les niveaux d’éosinophiles n’ont pas été utilisés pour le diagnostic de l’ECOPD ou la classification de la gravité.
La radiographie pulmonaire est utile pour différencier la pneumonie (et d’autres affections pouvant imiter l’ECOPD, comme le pneumothorax ou la pleurésie) de l’ECOPD et est fréquemment obtenue chez les patients traités dans des établissements de santé, mais cet outil n’a pas été utilisé pour définir ou classer la gravité de l’ECOPD. une ECOPD.
| En conclusion , en intégrant des variables cliniques et de laboratoire mesurables au moment de l’exacerbation, la proposition de Rome pour une définition actualisée de l’ECOPD pourrait aider à standardiser les soins et les résultats pour les cliniciens et les chercheurs. |















