Résumé Des essais cliniques récents menés auprès de personnes atteintes de diabète de type 2 ont démontré des effets bénéfiques sur les résultats cardiaques et rénaux après un traitement par agonistes des récepteurs GLP-1 (GLP-1RA). Ces actions sont en partie cohérentes avec un meilleur contrôle de la glycémie et une perte de poids significative. Mais les GLP-1RA peuvent également présenter des avantages supplémentaires en améliorant le dysmétabolisme postprandial. Dans le diabète, les fonctions nutritionnelles postprandiales dérégulées déclenchent une inflammation, un stress oxydatif, un dysfonctionnement endothélial, une thrombogénicité et une endotoxémie ; modifications des niveaux hormonaux; et la modulation du débit cardiaque et du flux sanguin et lymphatique régional. Dans cette perspective, nous explorons les actions des GLP-1RA à l’état postprandial et leur rôle potentiel dans les bénéfices sur les organes cibles observés dans des essais récents. |
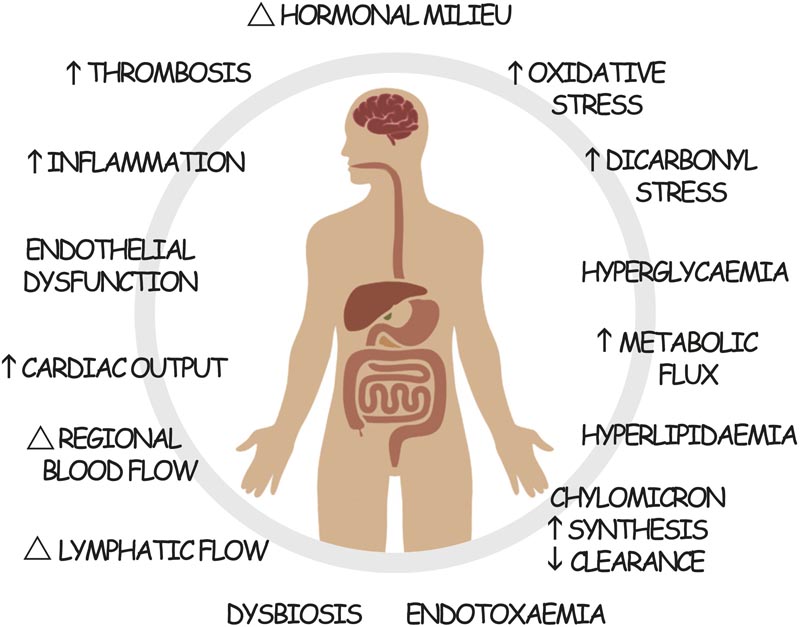
Le dysmétabolisme postprandial contribue au développement et à la progression des maladies cardiovasculaires et rénales dans le diabète de type 2. Chacun de ces mécanismes pathogènes peut être modifié par un traitement au GLP-1RA.
Il y a quatre-vingt-dix ans, LaBarre a décrit pour la première fois des « incrétines » contenues dans des extraits de muqueuse duodénale qui réduisaient les niveaux de glucose chez les chiens, soi-disant en augmentant la sécrétion d’insuline, d’où son nom (de la sécrétion intestinale d’insuline). ).
Les incrétines ont été conçues comme des équivalents endocriniens de la sécrétine, une hormone libérée par l’ intestin identifiée 30 ans plus tôt, avec des actions postprandiales pour réguler la sécrétion de liquide pancréatique et l’accommodation gastrique. La plus grande libération d’insuline (incrétine) en réponse à une provocation orale de glucose par rapport à la même charge de glucose administrée par voie intraveineuse est devenue plus tard connue sous le nom d’ « effet incrétine » , et le peptide de type glucagon-1 (GLP-1) 1) a été identifié plus tard. comme son principal médiateur insulinotrope.
En 1993, il a été démontré qu’une perfusion de GLP-1 pouvait réduire la glycémie chez les personnes atteintes de diabète de type 2 (DT2). Et plus récemment, des analogues du GLP-1 (à base d’exendine) et des versions à action prolongée du GLP-1 humain ont été développés pour une utilisation clinique dans le DT2 et l’obésité.
Les GLP-1RA sont désormais largement utilisés comme agents hypoglycémiants chez les personnes atteintes de DT2, où l’ajout d’un GLP-1RA au traitement standard réduit systématiquement l’HbA1c d’environ 1 %.5 Dans les essais cliniques comparatifs, les GLP-1RA obtiennent des réductions similaires ou supérieures. en HbA1c, en glycémie à jeun et en contrôle glycémique postprandial que l’insuline basale titrée ou la thérapie par bolus basal.
De plus, les GLP-1RA ont une charge de manipulation inférieure à celle de l’insuline, associée à un risque réduit d’hypoglycémie , à un manque de prise de poids et à un besoin réduit d’auto-surveillance du glucose ou de cohérence dans l’apport alimentaire en glucides. Pour ces raisons, et pour les avantages pour les organes cibles, les GLP-1RA sont désormais recommandés comme agent injectable préféré pour le traitement du DT2 par rapport à l’insuline dans la plupart des cas.
Plus récemment, les GLP-1RA se sont également révélés très efficaces pour induire une perte de poids , principalement grâce à un meilleur contrôle de l’appétit et de la satiété et à une réduction ultérieure de la consommation d’énergie. Même si une perte de poids modeste a été observée dans les essais menés chez des personnes atteintes de DT2, des études récentes utilisant des doses élevées de GLP-1RA chez des personnes obèses ont désormais démontré des changements très significatifs dans le poids corporel comme résultat principal. Par exemple, une étude récente a montré que près de 40 % des participants traités au sémaglutide une fois par semaine ont perdu plus de 20 % de leur poids corporel.
Cependant, les actions cliniques des GLP-1RA semblent être bien plus larges que la réduction de la glycémie ou l’induction d’une perte de poids. En particulier, de récents essais à grande échelle menés auprès de personnes atteintes de DT2 ont montré des bénéfices inattendus sur différents résultats cardiovasculaires et rénaux , en plus de ses actions évidentes dans l’amélioration du contrôle de la glycémie et la réduction du poids corporel. Dans cette perspective, nous proposons que les actions uniques du GLP-1RA sur le dysmétabolisme postprandial associé au DT2 (Figure 1) puissent conférer en partie ces bénéfices additifs.
Conclusions
Les GLP-1RA améliorent les résultats du MACE chez les personnes atteintes de DT2 présentant une maladie cardiovasculaire établie ou un risque cardiovasculaire élevé et sont désormais largement recommandés en complément des soins standard dans ce contexte.
Chez les patients atteints de DT2 et d’IRC, les GLP-1RA sont également recommandés, en partie en raison du risque cardiovasculaire élevé associé à l’IRC et du plus grand bénéfice absolu du traitement par GLP-1RA, ainsi que des preuves émergentes d’actions rénoprotectrices actuellement à l’étude. . Testé dans le cadre de grandes études spécifiques aux résultats rénaux. Dans chaque cas, les bénéfices des GLP-1RA semblent être largement conférés par un contrôle glycémique nettement meilleur et une perte de poids significative, qui sont reconnus comme des piliers clés de la prise en charge multifactorielle du DT2.
En outre, les agents qui permettent une réduction plus importante de la glycémie et une perte de poids semblent également avoir de plus grands avantages cardiovasculaires et rénaux. Mais en même temps, dans la mesure où ces actions reflètent la puissance de l’agent, les GLP-1RA qui sont plus efficaces pour abaisser le glucose ou favoriser la perte de poids pourraient logiquement également être plus efficaces pour améliorer les fonctions cardiovasculaires ou rénales en raison d’un mécanisme d’action partagé. (par exemple, activation du GLP-1R).
Cependant, ni la réduction de l’HbA1c ni la perte de poids ne semblent expliquer pleinement les bénéfices observés sur les organes cibles. Nous pensons que les instruments grossiers utilisés pour mesurer le contrôle du diabète (par exemple, HbA1c, lipides à jeun, poids corporel, tension artérielle en cabinet, etc.) ne parviennent pas à capturer de manière exhaustive l’activité complète du traitement du diabète. GLP-1RA. En particulier, nous émettons l’hypothèse que les actions (non mesurées) des GLP-1RA dans la modulation du dysmétabolisme postprandial dans le DT2 (Figure 1) pourraient contribuer aux avantages additifs apparents des GLP-1RA par rapport aux thérapies conventionnelles. de soins standards observés. En atténuant les pics de glucose et de lipides postprandiaux dérégulés et les poussées d’inflammation, de stress oxydatif, de dysfonctionnement endothélial, de thrombogénicité, d’endotoxémie et d’altération du flux sanguin et lymphatique régional qui en résultent, le développement et la progression des maladies cardiovasculaires et rénales peuvent être davantage ralenties.
Le mode de vie moderne malsain signifie qu’une grande partie de notre journée d’éveil se déroule désormais dans un état postprandial.
Durant cette période, les aliments transformés riches en graisses et/ou glucides et pauvres en fibres sont digérés. Le coût de ce mode de vie est potentiellement notre santé, notamment des taux plus élevés d’obésité, de DT2, d’ASCVD et d’IRC. Le chaînon manquant dans la gestion de ces conditions est de se concentrer sur les effets immédiats de nos aliments. Ce n’est pas une nouvelle idée. En fait, l’athérosclérose a été proposée comme phénomène postprandial en 1979.
Les effets du métabolisme postprandial soutiennent probablement les bienfaits observés pour la santé de la modification des macronutriments alimentaires, au-delà du contrôle du poids. De plus, les actions des fibres alimentaires et des micronutriments, tels que les polyphénols, les antioxydants et même l’éthanol, sur le métabolisme postprandial peuvent également expliquer en partie certains de leurs bienfaits cardiovasculaires et/ou rénaux. Il est donc plausible qu’au-delà des effets cumulatifs sur l’HbA1c ou le poids corporel, la modulation directe de l’état postprandial par les GLP-1RA joue également un rôle dans les bénéfices observés après un traitement par ces agents. . De plus, la signalisation centrale activée par les GLP-1RA module non seulement l’appétit et l’apport calorique, mais influence également de manière significative le choix ou la préférence alimentaire , afin de réduire la consommation d’aliments riches en graisses et en énergie.
Par exemple, le tirzépatide réduit la préférence pour les aliments riches en graisses et en calories de manière dépendante du GLP-1R. Dans le même temps, l’exénatide a accru les préférences pour les aliments faibles en calories, mesurées par l’activation cérébrale après la visualisation d’images de différents aliments. Le traitement GLP-1RA est capable de réduire les fringales et les grignotages entre les repas et module également la prise alimentaire hédonique . L’amélioration de l’environnement postprandial obtenue indirectement par la préférence et la sélection d’aliments plus sains avec une densité énergétique moindre peut être aussi importante pour le risque cardiovasculaire et rénal que toute action directe des GLP-1RA sur les mêmes risques, avec laquelle il existe une synergie évidente.
Le développement et l’évolution des GLP-1RA continuent de révolutionner la gestion du DT2, avec de plus en plus d’agonistes plus récents et plus puissants qui abaissent profondément les niveaux de glucose et entraînent des pertes substantielles d’excès de graisse corporelle. . Les actions pléiotropes des GLP-1RA dans le DT2, bien que significatives, sont probablement pâles en comparaison de la capacité des agents à mettre le DT2 ou l’obésité en « rémission » et des effets secondaires que cela aura sur la santé cardiovasculaire et rénale. . Cependant, l’amélioration de la compréhension de ces voies mènera probablement également à de nouvelles opportunités pour améliorer l’activité cardiovasculaire et rénale, au-delà du métabolisme, grâce à un agonisme des récepteurs plus puissant, une signalisation biaisée et des approches multirécepteurs hybrides pour mieux réguler l’état postprandial. L’activité clinique exceptionnelle déjà observée avec le tirzépatide , un agoniste puissant et biaisé du GLP-1R et du GIP-R, n’est qu’un avant-goût de la révolution thérapeutique à venir.
















