Résumé Pendant la propagation du coronavirus-2 du syndrome respiratoire aigu sévère, certains rapports de données encore émergents et nécessitant une analyse complète indiquent que certains groupes de patients sont à risque de contracter le COVID-19. Cela inclut les patients souffrant d’hypertension, de maladies cardiaques, de diabète sucré et clairement les personnes âgées. Beaucoup de ces patients sont traités avec des bloqueurs du système rénine-ngiotensine . Parce que la protéine ACE2 (enzyme de conversion de l’angiotensine 2) est le récepteur qui facilite l’entrée du coronavirus dans les cellules, l’idée est devenue populaire selon laquelle un traitement par des bloqueurs du système rénine-angiotensine pourrait augmenter le risque de développer une infection. en raison d’un coronavirus aigu grave et mortel. Cet article traite de ce concept . L’ACE2 dans sa forme complète est une enzyme liée à la membrane, tandis que sa forme plus courte (soluble) circule dans le sang à des niveaux très faibles. En tant que monocarboxypeptidase, ACE2 contribue à la dégradation de plusieurs substrats, dont les angiotensines I et II. je Les inhibiteurs de l’ECA (enzyme de conversion de l’angiotensine) n’inhibent pas l’ACE2 car l’ACE et l’ACE2 sont des enzymes différentes. Bien qu’il ait été démontré que les bloqueurs des récepteurs de l’angiotensine II de type 1 régulent positivement l’ACE2 chez les animaux de laboratoire, les preuves ne sont pas toujours cohérentes et diffèrent entre les divers bloqueurs des récepteurs de l’angiotensine II de type 1 et les différents organes. De plus, il n’existe aucune donnée pour étayer l’idée selon laquelle l’administration d’inhibiteurs de l’ECA ou d’inhibiteurs des récepteurs de l’angiotensine II de type 1 facilite l’entrée du coronavirus en augmentant l’expression de l’ACE2 chez les animaux ou les humains. En effet, les données animales soutiennent une expression élevée de l’ACE2, conférant des effets protecteurs pulmonaires et cardiovasculaires potentiels. En résumé, sur la base des preuves actuellement disponibles, le traitement par les bloqueurs du système rénine-angiotensine ne doit pas être interrompu en raison de préoccupations liées à une infection par le coronavirus. |
La propagation du coronavirus-2 du syndrome respiratoire aigu sévère (SRAS-CoV-2) a déjà pris des proportions pandémiques, ayant infecté plus de 100 000 personnes dans 100 pays. Bien que l’objectif principal actuel des autorités de santé publique soit de développer une réponse mondiale coordonnée pour préparer les systèmes de santé à relever ce défi sans précédent, une préoccupation a été identifiée qui intéresse particulièrement les cliniciens et les chercheurs s’intéressant fortement à l’hypertension artérielle.
L’hypertension, les maladies coronariennes et le diabète sucré, en particulier chez les personnes âgées, augmentent la susceptibilité à l’infection par le SRAS-CoV-2.
Puisque l’ACE2 (enzyme de conversion de l’angiotensine 2) est le récepteur qui permet au coronavirus de pénétrer dans les cellules, l’idée a émergé que l’utilisation préexistante d’inhibiteurs du système rénine-angiotensine (RAS) pourrait augmenter le risque de développer une infection grave. et mortel du SRASCoV-2.
Ce commentaire discute de cette préoccupation et conclut que, sur la base des preuves actuelles, il n’y a aucune raison d’abandonner les bloqueurs du SRA chez les patients recevant cette classe importante d’agents antihypertenseurs en raison des craintes d’un risque accru de contracter le SRAS-CoV-2 ou d’aggraver son évolution. .
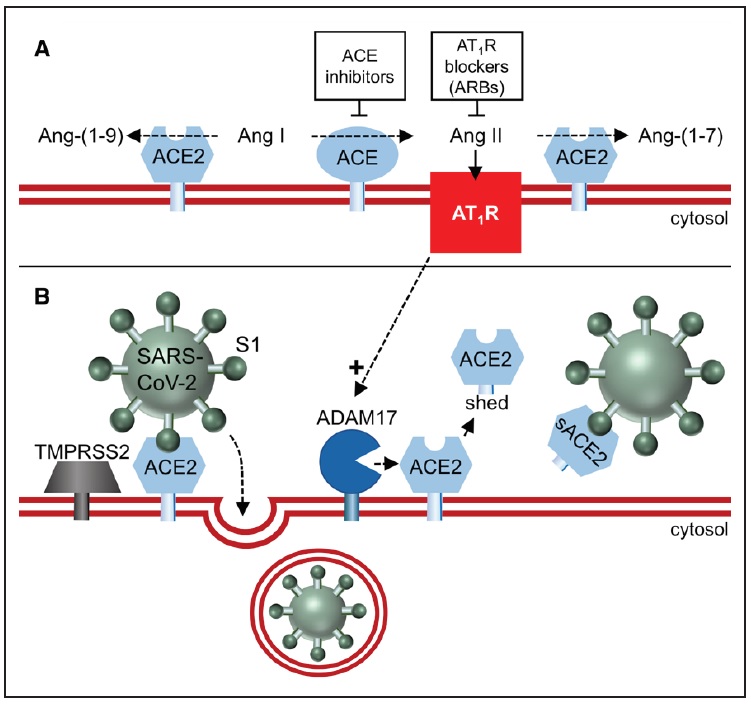 Chiffre. La carboxypeptidase ACE2 (enzyme de conversion de l’angiotensine 2) convertit l’Ang II (angiotensine II) en Ang-(1-7) et l’Ang I en Ang-(1-9)(A), mais n’est pas bloquée par l’ACE (enzyme de conversion de l’angiotensine ), qui empêchent la conversion de Ang I en Ang II. ACE2 se lie et internalise également SARSCov-2 (coronavirus-2 du syndrome respiratoire aigu sévère ; B), après amorçage avec la sérine protéase TMPRSS2 (protéase transmembranaire, sérine 2). L’élimination de l’ACE2 lié à la membrane par une désintégrine et une métalloprotéase 17 (ADAM17) entraîne l’apparition d’ACE2 solubles, qui ne peuvent plus médier l’entrée de SARSCov-2 et pourraient même empêcher une telle entrée en maintenant le virus en solution. AT1R (Ang II, via son récepteur de type 1) régule positivement ADAM17, et les bloqueurs d’AT1R (ARB) empêcheraient cela.
Chiffre. La carboxypeptidase ACE2 (enzyme de conversion de l’angiotensine 2) convertit l’Ang II (angiotensine II) en Ang-(1-7) et l’Ang I en Ang-(1-9)(A), mais n’est pas bloquée par l’ACE (enzyme de conversion de l’angiotensine ), qui empêchent la conversion de Ang I en Ang II. ACE2 se lie et internalise également SARSCov-2 (coronavirus-2 du syndrome respiratoire aigu sévère ; B), après amorçage avec la sérine protéase TMPRSS2 (protéase transmembranaire, sérine 2). L’élimination de l’ACE2 lié à la membrane par une désintégrine et une métalloprotéase 17 (ADAM17) entraîne l’apparition d’ACE2 solubles, qui ne peuvent plus médier l’entrée de SARSCov-2 et pourraient même empêcher une telle entrée en maintenant le virus en solution. AT1R (Ang II, via son récepteur de type 1) régule positivement ADAM17, et les bloqueurs d’AT1R (ARB) empêcheraient cela.
Coronavirus et ACE2
En 2003, Li et al4 ont démontré que l’ACE2 est le récepteur responsable de l’entrée du coronavirus du SRAS. La liaison au récepteur ACE2 nécessite l’unité de surface d’une protéine de pointe virale. L’entrée cellulaire ultérieure dépend de l’amorçage par la sérine protéase TMPRSS2 (protéase transmembranaire, sérine 2). Deux rapports récents ont confirmé que le SRAS-CoV-2 pénètre également dans la cellule par cette voie. Il est important de noter que l’entrée du SRAS-CoV-2 dans la cellule pourrait être bloquée à la fois par les anticorps neutralisant la protéine S et par les inhibiteurs de TMPRSS2 (mésylate de camostat).
Dans les poumons, l’expression de l’ACE2 se produit dans les pneumocytes et les macrophages de type 2. En général, cependant, l’expression pulmonaire de l’ACE2 est faible par rapport à d’autres organes tels que l’intestin, les testicules, le cœur et les reins.
ACE2 présente une homologie considérable avec l’ACE (enzyme de conversion de l’angiotensine ; 40 % d’identité et 61 % de similarité) et, sur cette base, a été nommée en 2000. En tant que monocarboxypeptidase, elle hydrolyse plusieurs peptides, notamment l’apéline, les opioïdes, les kinines et les angiotensines. Une grande partie des travaux sur ACE2 s’est concentrée sur les effets biologiques liés à la formation d’angiotensine-(1-7) à partir de l’angiotensine II.
Contrairement à l’ACE, l’ACE2 ne convertit pas l’angiotensine I en angiotensine II et les inhibiteurs de l’ECA ne bloquent pas non plus son activité.
Ceci n’est pas surprenant car l’homologie ne concerne pas le site actif. L’ACE2 est la plus puissante des 3 enzymes connues pour convertir l’angiotensine II vasoconstrictrice en angiotensine-(1-7). L’angiotensine-(1-7) possède de plus en plus de propriétés protectrices d’organes qui s’opposent et contrecarrent celles de l’angiotensine II.
Le récepteur AT1 (angiotensine II, via son type 1) régule positivement ADAM17, augmentant ainsi les niveaux d’ACE2 soluble. Dans l’urine, les niveaux solubles d’ACE2 peuvent être importants et résultent probablement de la desquamation de la membrane tubulaire proximale.
Quels sont les effets des bloqueurs du RAS sur l’ACE2 ?
C’est vraiment le nœud de la question et la confusion et la panique dominantes auxquelles nous assistons dans la communauté médicale après la propagation de la rumeur selon laquelle l’ACE2 est le récepteur du SRAS-CoV-2. Une partie de la confusion qui règne sur les réseaux sociaux et dans le grand public est due au fait que les inhibiteurs de l’ECA sont parfois confondus avec les inhibiteurs de l’ACE2. Il s’agit de 2 enzymes différentes avec 2 sites actifs différents et tout effet de l’ACE, donc les inhibiteurs de l’activité ACE2 doivent être indirects, via leurs substrats respectifs. Il est peu probable que cela ait un lien avec la liaison du SRAS-CoV-2. Cependant, peu de rapports indiquent que les inhibiteurs de l’ECA affectent l’expression de l’ACE2 dans le cœur et les reins.
Les bloqueurs des récepteurs AT1 (ARA) modifient l’expression de l’ACE2 de manière plus cohérente dans plusieurs études, tant au niveau de l’ARNm que des protéines. Il a été mieux documenté dans le tissu cardiaque et le système vasculaire rénal. Cependant, même dans ce cas, les résultats sont mitigés, nécessitent des doses élevées et diffèrent souvent selon les ARA et les organes.
Dans l’ensemble, il existe des preuves issues d’études animales selon lesquelles les ARA peuvent réguler positivement l’ACE2 lié à la membrane, alors que les inhibiteurs de l’ECA ne le peuvent pas. Cependant, les données actuelles sont souvent contradictoires et varient selon les ARA et les tissus (p. ex., cœur ou rein). Même si la régulation positive rapportée de l’ACE2 tissulaire par les ARA dans les études animales et généralement à des doses élevées pouvait être extrapolée à l’homme, cela ne permettrait pas d’établir qu’elle est suffisante pour faciliter l’entrée du SRAS-CoV-2.
Nous tenons à souligner qu’un effet pulmonaire potentiellement bénéfique des ARA doit également être pris en compte. Lors d’une lésion pulmonaire aiguë, l’ACE2 alvéolaire semble être régulée négativement. Cela diminuerait le métabolisme de l’angiotensine II, entraînant une augmentation des niveaux locaux de ce peptide, augmentant la perméabilité alvéolaire et favorisant les lésions pulmonaires. Dans ce contexte, on peut supposer qu’une augmentation de l’expression de l’ACE2 par un traitement ARB préexistant pourrait en fait avoir un effet protecteur au cours de l’infection par le SRAS-CoV-2.
Risques d’abandon du traitement ACEI/ARB chez les patients atteints de coronavirus
| On ne sait pas exactement comment l’hypertension a été codée dans le récent rapport SARSCoV-21 : nous ne pouvons que spéculer sur le fait que cela pourrait être basé sur l’utilisation de médicaments contre l’hypertension plutôt que sur la mesure réelle de la pression artérielle. |
Pour véritablement déterminer si les patients souffrant d’hypertension sont plus susceptibles de développer des infections graves et mortelles au SRASCoV-2, une étude de cohorte prospective avec les taux d’incidence de l’infection par le SRAS-CoV-2 dans une cohorte de patients souffrant d’hypertension et de patients est nécessaire. sans hypertension , avec des antécédents d’exposition similaires. Au lieu de cela, ce qui a été rapporté est un antécédent d’hypertension versus non , chez les patients atteints du SRAS-CoV-2, sans aucun ajustement (par exemple, en fonction de l’âge).
L’utilisation des bloqueurs du SRA comme lien de causalité est une hypothèse qui manque de preuves , comme discuté ici. Par conséquent, nous recommandons fortement aux patients prenant des inhibiteurs de l’ECA ou des ARA pour traiter l’hypertension artérielle, l’insuffisance cardiaque ou d’autres indications médicales de ne pas interrompre leur traitement actuel, sauf sur recommandation spécifique de leur médecin ou professionnel de la santé. . Il y a un avertissement supplémentaire. Toute déstabilisation du contrôle de la pression artérielle en cas d’hypertension, qui pourrait survenir suite à des changements de médicaments, entraînerait des risques inacceptables d’accidents vasculaires cérébraux et de crises cardiaques précipitées, risques qui ne sont évidemment pas seulement hypothétiques. L’arrêt pur et simple des antihypertenseurs est déconseillé et ne devrait pas être une option, compte tenu de l’utilisation répandue des bloqueurs du SRA dans le monde entier. En particulier, les Asiatiques semblent être plus enclins à tousser et les ARA pourraient donc être préférables. |
Prochaines étapes
La base de données cliniques disponible à ce jour sur la pandémie est insuffisante pour fournir suffisamment de détails sur les variables d’intérêt : diagnostic d’hypertension et médicaments antihypertenseurs prescrits pour tester les hypothèses proposées et apporter une certitude. Ces informations sont donc désespérément nécessaires.
Bien qu’aucun traitement n’ait actuellement été établi pour les patients atteints du SARSCoV-2, le domaine évolue rapidement et des approches potentielles sont à l’étude. Ceux-ci incluent des antiviraux à large spectre tels que le favipiravir et le remdesivir, l’inhibition de TMPRSS2 avec le mésylate de camostat et la régulation positive d’ADAM17.
Une approche plus ciblée pourrait consister à utiliser la protéine ACE2 recombinante soluble pour empêcher le virus de se lier à l’ACE2 complet ancré dans la membrane plasmique cellulaire. Ces approches sont les plus judicieuses pour le traitement des patients présentant un risque élevé de syndrome de détresse respiratoire aiguë. À des fins préventives, l’objectif est bien entendu le développement d’un vaccin contre le SRAS-CoV-2.
En conclusion, nous ne voyons aucune raison d’abandonner ou de suspendre temporairement l’utilisation préventive des bloqueurs du SRA chez les patients atteints du SARSCoV-2.
Certains craignent que ces agents, en particulier les ARA, puissent affecter l’expression de l’ACE2 sur la base de modèles animaux qui, cependant, n’ont pas été confrontés à une infection à coronavirus pour évaluer l’impact du traitement bloquant le RAS. Puisque cette information fait défaut, nous ne voyons aucune raison de paniquer et de modifier la prescription de cette classe d’antihypertenseurs d’une importance cruciale.
Son bénéfice thérapeutique l’emporte, selon nous, sur tout risque potentiel de prédisposition à l’infection par le coronavirus. De plus, on ne sait pas si les médicaments antihypertenseurs alternatifs ne comportent pas le même risque.
Une autre question est de savoir que faire chez les personnes infectées risquant d’évoluer vers une insuffisance rénale terminale. La décision ici doit être basée sur le jugement clinique et prendre en compte les avantages et les inconvénients du blocage du SRA chez les patients gravement malades, tels que la présence ou l’absence d’hypotension et l’effet possible sur la fonction rénale.
Messages pour la pratique
|