Einführung
Trigeminusneuralgie, traditionell Tic douloureux genannt, ist eine chronische neuropathische Schmerzstörung , die durch spontane und provozierte Anfälle stechender oder stromschlagartiger Schmerzen in einer Gesichtsregion gekennzeichnet ist. Eine schlechte Lebensqualität und in schweren Fällen Selbstmord wurden auf die Störung zurückgeführt.
Klinische Merkmale und Diagnose
Die Diagnose einer Trigeminusneuralgie erfolgt klinisch und basiert auf drei Hauptkriterien:
- Schmerzen, die auf das Gebiet eines oder mehrerer Abschnitte des Trigeminusnervs beschränkt sind.
- Schmerzanfälle, die plötzlich, intensiv und sehr kurz auftreten (weniger als 1 Sekunde bis 2 Minuten, normalerweise jedoch einige Sekunden) und als „Schock“ oder „elektrisches Gefühl“ beschrieben werden.
- Schmerzen, die durch harmlose Reize im Gesicht oder im intraoralen Trigeminusgebiet ausgelöst werden.
Paroxysmal ausgelöste Schmerzen treten insbesondere bei der Trigeminusneuralgie auf und werden von 91 bis 99 % der Patienten berichtet, was darauf hindeutet, dass dieses Merkmal pathognomonisch für die Trigeminusneuralgie sein könnte.
Trigeminusneuralgie-Schmerzen betreffen am häufigsten die Verteilung des zweiten (Oberkiefer) oder dritten (Unterkiefer) Abschnitts des Trigeminusnervs und betreffen die rechte Gesichtshälfte häufiger als die linke.
Eine beidseitige Trigeminusneuralgie ist selten und sollte Anlass zur Sorge hinsichtlich der Möglichkeit einer Gesichtsneuralgie aufgrund einer neurologischen Grunderkrankung oder einer nicht-neurologischen Erkrankung des Schädels geben.
Die Inzidenz einer Trigeminusneuralgie ist bei Frauen höher als bei Männern und nimmt mit zunehmendem Alter zu.
Viele Formen von Gesichtsschmerzen wurden mit Trigeminusneuralgie kombiniert, es handelt sich jedoch wahrscheinlich um unterschiedliche Entitäten, die manchmal in die Kategorie „atypischer Gesichtsschmerz“ oder „schmerzhafte Trigeminusneuropathie “ eingeordnet werden.
Das hintere Drittel der Kopfhaut, das äußere Ohr (mit Ausnahme des Tragus) und die Haut über dem Kieferwinkel werden nicht vom Nervus trigeminus innerviert und sind keine Schmerzherde aufgrund einer Trigeminusneuralgie (siehe Abbildung unten); Schmerzen in diesen Bereichen deuten auf einen anderen Prozess hin.
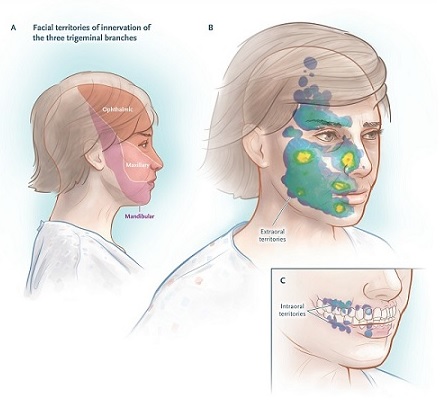
Innervationsgebiete des Trigeminusnervs und Verteilung der Aktivierungszone.
Der Schmerz einer Trigeminusneuralgie kann durch alltägliche Gesten ausgelöst werden. Die Auslöser finden sich in kleinen rezeptiven Sinneszonen, beispielsweise der Berührung einer Serviette oder eines Taschentuchs auf der Oberlippe oder sogar einer durch einen empfindlichen Bereich strömenden Brise des Gesichts.
Der Ort des Schmerzes stimmt nicht immer mit dem Ort des sensorischen Auslösers überein. Beispielsweise können Reize in und um die Unterlippe Schmerzen in der Schläfe hervorrufen, oder sensorische Auslöser in den seitlichen Teilen der Nase können schockartige Schmerzen hervorrufen, die auf die Stirn oder die Oberlippe ausstrahlen.
Die spezifischen Aktivierungsmanöver einer Reihe von Patienten sind in der folgenden Tabelle dargestellt, und die Verteilung der Aktivierungszonen, die Schmerzen verursachen, ist in der Abbildung oben dargestellt. Nur wenige Patienten berichten über keine Auslöser.
Die Untersuchung einer Trigeminusneuralgie umfasst die Beobachtung des Gesichts, während der Patient völlig still sitzt. Bei einem spontanen Anfall einer Trigeminusneuralgie kann der Arzt ein Blinzeln oder eine kleine Bewegung des Mundes bemerken, die dem Patienten unbekannt ist.
Seltener kann es während eines paroxysmalen Anfalls zu einer heftigen Kontraktion der Gesichtsmuskeln kommen, die als „Tic-Krampf“ bezeichnet wird. Die sensorische Untersuchung des Gesichts ist bei Trigeminusneuralgie im Allgemeinen nicht aufschlussreich, obwohl einige Patienten über Bereiche mit leichter Hypästhesie berichten.
Arten und Ursachen
Drei Arten der Trigeminusneuralgie wurden unterschieden: klassische, sekundäre und idiopathische. Der klassische Typ , der am häufigsten vorkommt, wird durch eine intrakranielle Gefäßkompression der Trigeminuswurzel verursacht , wie unten beschrieben. Das verantwortliche Gefäß ist in der Regel die Arteria cerebellaris superior , die morphologische Veränderungen in der angrenzenden Wurzel des Trigeminusnervs induziert.
Die sekundäre Trigeminusneuralgie , die etwa 15 % der Fälle ausmacht, ist auf eine erkennbare neurologische Erkrankung wie Multiple Sklerose oder einen Tumor im Kleinhirnbrückenwinkel zurückzuführen, der die Eintrittszone der Trigeminuswurzel verändert oder den Nerv in seinem extrakraniellen Teil komprimiert.
Die idiopathische Trigeminusneuralgie, bei der keine erkennbare Ursache gefunden werden kann, macht etwa 10 % der Fälle aus.
Die klinischen Merkmale der klassischen und sekundären Trigeminusneuralgie sind ähnlich, allerdings sind Patienten mit sekundärer Trigeminusneuralgie tendenziell jünger , leiden häufiger an einem Gefühlsverlust in einem Teil des Gesichts und haben häufiger beidseitige Schmerzen .
Da die drei Formen der Trigeminusneuralgie klinisch möglicherweise nicht unterscheidbar sind, ist es ratsam, zum Zeitpunkt der Erstdiagnose eine Gadolinium-Magnetresonanztomographie (MRT) durchzuführen, um Multiple Sklerose und Kleinhirnbrückentumoren auszuschließen.
Eine kürzlich durchgeführte Studie zeigte seltene Varianten in Genen, die spannungsgesteuerte Ionenkanäle bei Patienten mit einer Familienanamnese von klassischer oder idiopathischer Trigeminusneuralgie kodieren. Die Häufigkeit und klinische Bedeutung dieses Befundes ist jedoch unbekannt.
Neurovaskuläre Kompression bei klassischer Trigeminusneuralgie
In den letzten Jahrzehnten wurde die klassische Form der Trigeminusneuralgie durch die Arbeit von Jannetta et al. entdeckt und das Heilungspotenzial durch intrakranielle mikrovaskuläre Chirurgie untersucht.
Als Pathophysiologie wird eine Kompression des sensorischen Teils des Nervus trigeminus in der Nähe seines Eintrittsbereichs in die Pons durch einen kleinen angrenzenden Ast der Arteria basilaris, meist der Arteria cerebellaris superior , angesehen . Allerdings scheint ein einfacher Kontakt zwischen dem Nerv und einer Gefäßstruktur nicht ausreichend zu sein, um die Störung zu verursachen oder zu erklären.
Um die Störung auf eine neurovaskuläre Kompression zurückzuführen , wäre es ideal, nachzuweisen, dass das anomale Gefäß anatomische Veränderungen in der Trigeminuswurzel induziert, wie z. B. eine Verformung oder Atrophie. Der charakteristischste Befund während der Operation ist eine kleine gewundene Arterie oder Arterienschlinge, die in ihrem Eintrittsbereich auf die mediale Seite der Trigeminuswurzel trifft und zu einer seitlichen Luxation, Verformung, Abflachung oder Atrophie der Nervenwurzel führt.
Eine neurovaskuläre Kompression kann mithilfe von MRT und dreidimensionaler Rekonstruktion beobachtet werden. Zu den bildgebenden Verfahren gehören dreidimensionale T2-MRT-Sequenzen mit detaillierter Untersuchung der Zisternen- und Schwellkörpersegmente des Nervs, dreidimensionale Magnetresonanzangiographie zur Visualisierung von Arterien und Phasenkontrast-MRT zur Darstellung von Venen.
Eine Gefäßdekompression kann diese Anomalien in der Wurzeleintrittszone des Trigeminus umkehren, wo der sensorische Teil des Nervs in die Brücke eintritt.
Pathophysiologie
An seinem Eingang zur Pons verliert der Trigeminusnerv (wie alle peripheren Nerven) seine Myelinscheide aus Schwann-Zellen und wird durch zentrales Myelin ersetzt, das von Oligodendroglia erzeugt wird.
Diese Übergangszone ist anfällig für Schäden und insbesondere für Demyelinisierung . Gefäßkompression ist die übliche Ursache für eine Demyelinisierung, bevor der Nerv in die Pons eintritt, und Multiple Sklerose ist die typische Ursache direkt nach dem Eintritt in die Pons. Eine Demyelinisierung an diesen Stellen wurde in neurophysiologischen, bildgebenden und histologischen Studien nachgewiesen.
Wenn die Myelinscheide dünn genug wird, um den transmembranären Durchgang von Ionen in das darunter liegende Axon zu ermöglichen, ist das Axon nicht in der Lage, Natrium schnell zu pumpen.
Durch die daraus resultierende Depolarisation wird das Axon übererregbar , was zu einer ektopischen Erzeugung von Impulsen mit hochfrequenten Nachentladungen (Entladungen, die nach Beendigung des Reizes auftreten) und Übersprechen zwischen Fasern (sogenannte ephaptische Übertragung) führt. Histologische Erkenntnisse deuten darauf hin, dass die an der Demyelinisierung am stärksten beteiligten Nervenfasern A-β-Fasern (große, nicht nozizeptive Fasern) sind, die am anfälligsten für eine Demyelinisierung aufgrund mechanischer Schäden oder Multipler Sklerose sind.
Es wurde vorgeschlagen, dass hochfrequente Entladungen, die an der Demyelinisierungsstelle entlang der primären A-β-Afferenzen entstehen, von Hirnstammneuronen umgeleitet werden , um als paroxysmaler Schmerz wahrgenommen zu werden .
Einige Forscher haben bei Patienten mit Trigeminusneuralgie eine übermäßige Erregbarkeit oder eine Verringerung des Volumens mehrerer kortikaler und subkortikaler Gehirnbereiche beobachtet. Diese Veränderungen sind jedoch wahrscheinlich eine Folge der Anpassung dieser Regionen an die chronische Stimulation.
Trigeminusneuralgie mit anhaltenden Schmerzen
Obwohl paroxysmale Gesichtsschmerzen das Kennzeichen der Trigeminusneuralgie sind, berichten 24 bis 49 % der Patienten über anhaltende oder anhaltende Schmerzen zwischen paroxysmalen Anfällen.
Schwankende Hintergrundschmerzen mit einer Verteilung, die mit der von paroxysmalen Schmerzen übereinstimmt, werden als brennender, pochender Schmerz oder Schmerz beschrieben . Eine Trigeminusneuralgie, die unabhängig von der Ursache durch dieses Symptom gekennzeichnet ist, wurde früher als Typ 2 oder atypische Trigeminusneuralgie klassifiziert und wird nun als Trigeminusneuralgie mit begleitenden anhaltenden Schmerzen klassifiziert .
Der Mechanismus, der dem anhaltenden Schmerz zugrunde liegt, unterscheidet sich vom Mechanismus, der dem paroxysmalen Schmerz zugrunde liegt, was durch die geringere Linderung des anhaltenden Schmerzes im Vergleich zum paroxysmalen Schmerz nach einer Behandlung mit Natriumkanalblockern oder einer mikrovaskulären Dekompression nahegelegt wird.
Der pathophysiologische Zusammenhang zwischen den beiden Schmerzentitäten ist ungewiss. Es wurden progressive Nervenwurzelschäden und zentrale Sensibilisierungsmechanismen vermutet. Brennende, stechende oder schmerzende Schmerzen werden wahrscheinlich durch eine Beeinträchtigung der C-Fasern (nicht myelinisierte sensorische Axone, die Impulse langsam übertragen) verursacht, wie dies bei anderen neuropathischen Schmerzzuständen der Fall ist.
Der Verlust von C-Fasern in der Trigeminus-Sinneswurzel kann zu abnormaler spontaner Aktivität in Neuronen zweiter Ordnung im Hirnstamm führen. Die bisherige Annahme, dass anhaltende Schmerzen als Folge einer langjährigen Trigeminusneuralgie entstehen, wird durch neuere Daten nicht gestützt.
Sekundäre Trigeminusneuralgie
Bei 15 % der Patienten mit typischen Schmerzattacken liegt der Trigeminusneuralgie eine Multiple Sklerose oder gutartige Tumoren im Kleinhirnbrückenwinkel zugrunde. Das Risiko einer Trigeminusneuralgie ist bei Patienten mit Multipler Sklerose im Vergleich zur Allgemeinbevölkerung um das Zwanzigfache erhöht, wobei die Prävalenz bei Patienten mit Multipler Sklerose bei 2 bis 5 % liegt.
Trigeminusneuralgie manifestiert sich manchmal als klinisch isoliertes Syndrom bei Patienten mit Multipler Sklerose; Das Erkrankungsalter der Multiplen Sklerose ist bei diesen Patienten höher als bei Patienten ohne Trigeminusneuralgie.
Eine Neuroimaging-Studie hat einen Zusammenhang zwischen neurovaskulärer Kompression und Trigeminusneuralgie im Zusammenhang mit Multipler Sklerose gezeigt, was darauf hindeutet, dass sie möglicherweise nebeneinander bestehen und sich addieren. Die Häufigkeit dieses dualen Mechanismus ist unbekannt, er hat jedoch Auswirkungen auf die Behandlung.
Die pharmakologische Behandlung von Trigeminusneuralgie-Schmerzen bei Patienten mit Multipler Sklerose stellt eine Herausforderung dar, da die Medikamente Nebenwirkungen haben, sich die Multiple-Sklerose-Symptome wie Müdigkeit und Ataxie verschlimmern und ihre Wirksamkeit bei solchen Patienten nur begrenzt nachgewiesen ist.
Fallstudien deuten darauf hin, dass chirurgische Eingriffe zur Reduzierung der Gefäßkompression tendenziell weniger wirksam sind als bei Patienten mit klassischer Trigeminusneuralgie.
Zu den Tumoren im Kleinhirnbrückenwinkel , die die Wurzel des Trigeminusnervs komprimieren und eine Trigeminusneuralgie verursachen, gehören Akustikusneurinome, Meningeome, Epidermoidzysten und Cholesteatome. Interessanterweise wurden Trigeminusneuralgien (die selten sind) nicht mit einer Trigeminusneuralgie in Verbindung gebracht.
In einer Analyse der Daten aus vier Studien, die 243 Patienten mit Trigeminusneuralgie umfassten, waren Tumore bei 20 Patienten (8 %) die Ursache. Die Kompression des Trigeminusnervs durch Tumore induziert eine fokale Demyelinisierung der Wurzel des Trigeminusnervs und löst die gleiche Erzeugung hochfrequenter Entladungen in nackten Axonen aus, die bei der Gefäßkompression des Nervs auftreten. Auch infiltrierende bösartige Tumoren können eine axonale Degeneration verursachen, was zu Hypästhesie in Gesichtsregionen und anhaltenden Schmerzen führt.
Trigeminusneuropathien aufgrund von Traumata und rheumatologischen Erkrankungen wie systemischem Lupus erythematodes und Sklerodermie können sich als paroxysmale Schmerzen manifestieren, die eine Trigeminusneuralgie imitieren, diese Assoziationen sind jedoch selten.
Gesichtstraumata, zahnärztliche Eingriffe oder Kiefer- und Gesichtsoperationen können Äste des Trigeminusnervs schädigen und ein paroxysmales Stechen verursachen, ähnlich einem Stromschlag oder brennenden Schmerzen. Allerdings dauern Schmerzattacken länger als Trigeminusneuralgie-Anfälle und die meisten Patienten beschreiben auch anhaltende starke Schmerzen ohne sensorische Triggerzonen.
Die isolierte idiopathische Trigeminusneuropathie, eine gutartige, bilaterale, symmetrische, rein sensorische Neuropathie, und die im Gesicht beginnende sensorische motorische Neuropathie, eine schwerwiegendere fortschreitende Erkrankung, können sich zunächst auch als einseitiger paroxysmaler Gesichtsschmerz manifestieren.
Hornhautreflextests werden als neurophysiologische Technik zur Erkennung einer Schädigung des Trigeminusnervs eingesetzt.
Dieser diagnostische Test ist nützlich bei Patienten, die sich keiner MRT unterziehen können, oder zum Nachweis von Demyelinisierung und Neuropathien, die eine Trigeminusneuralgie imitieren.
Behandlung
Medizinische Behandlung
Die Antikonvulsiva Carbamazepin in Dosen von etwa 200 bis 1.200 mg pro Tag und Oxcarbazepin (300 bis 1.800 mg pro Tag) gelten unabhängig von der Ursache als Erstbehandlung zur Kontrolle paroxysmaler Schmerzen bei Patienten mit Trigeminusneuralgie , mit deutlicher Schmerzkontrolle bei fast 90 % der Patienten.
Es wird angenommen, dass der Behandlungseffekt mit der Blockade spannungsgesteuerter Natriumkanäle zusammenhängt, was zur Stabilisierung übererregter neuronaler Membranen und zur Hemmung des wiederholten Feuerns führt.
Eine klinische Besserung geht jedoch häufig mit Nebenwirkungen einher, darunter Schwindel, Diplopie, Ataxie und erhöhte Aminotransferase-Werte, die bei 23 % der Patienten zum Abbruch der Behandlung führen können.
Oxcarbazepin hat möglicherweise weniger Nebenwirkungen als Carbamazepin, obwohl es aufgrund einer übermäßigen Depression des Zentralnervensystems oder einer dosisabhängigen Hyponatriämie abgesetzt werden kann.
Kontraindikationen für den Einsatz von Natriumkanalblockern sind Erregungsleitungsstörungen des Herzens und allergische Reaktionen mit einem hohen Grad an Kreuzreaktivität (40 bis 80 %) mit aromatischen Antiepileptika.
Carbamazepin und Oxcarbazepin reduzieren die hochfrequenten Entladungen, die schockartige Anfälle charakterisieren, die Wirkung dieser Medikamente auf die damit einhergehenden Dauerschmerzen ist jedoch meist begrenzt.
Gabapentin, Pregabalin und Antidepressiva, die sich bei der Behandlung anderer neuropathischer Erkrankungen, die durch anhaltende Schmerzen gekennzeichnet sind, als wirksam erwiesen haben, können als zusätzliche Wirkstoffe zusammen mit Oxcarbazepin oder Carbamazepin ausprobiert werden.
Klinische Erfahrungen deuten darauf hin, dass Gabapentin möglicherweise eine geringere Wirkung auf Trigeminusneuralgie hat als Carbamazepin und Oxcarbazepin, aber mit einer geringeren Inzidenz unerwünschter Ereignisse verbunden ist und als Monotherapie oder als Zusatztherapie versucht werden kann, selbst bei Patienten mit Multipler Sklerose. .
Wenn eine medikamentöse Behandlung wirkungslos ist oder mit inakzeptablen Nebenwirkungen einhergeht, kann eine chirurgische Dekompression des Trigeminusnervs in Betracht gezogen werden.
Lokale chirurgische Eingriffe
Obwohl chirurgische Eingriffe die Schwere und Häufigkeit von Trigeminusneuralgie-Anfällen bei entsprechend ausgewählten Patienten wirksam reduzieren, wird diese Art von Operation normalerweise nur durchgeführt, wenn Standarddosen von Medikamenten nicht ausreichen, um die Symptome zu kontrollieren, oder wenn die Nebenwirkungen eine weitere Anwendung verhindern.
Eine Gruppe chirurgischer Eingriffe, die heute nur noch selten durchgeführt werden, umfasst die periphere Blockade der Äste des Trigeminusnervs, wenn diese aus den Gesichtsknochen austreten, durch Neurektomie, Alkoholinjektionen oder die Induktion von Hochfrequenzläsionen oder Kryoläsionen.
Der Zweck dieser Verfahren besteht darin, im Gesicht einen Anästhesiebereich zu erzeugen, der der Verteilung des geschädigten Nervs entspricht. Allerdings wurde der Nutzen solcher Behandlungen durch Studien nicht ausreichend belegt und die Eingriffe führten oft zu schmerzhaften Narkosen (starke Schmerzen im Bereich des Sinnesverlustes).
Eine zweite Gruppe von Eingriffen zielt darauf ab, das Ganglion trigeminale im Cavum Meckel oder den Ausgang der Ganglionäste an der Schädelbasis perkutan zu schädigen, und zwar mittels Hochfrequenz-Thermokoagulation, chemischer Zerstörung durch Injektion von Glycerin oder Kompressionsmechanik durch Ballonaufblasen.
Die Radiofrequenz-Thermokoagulation schädigt vorzugsweise schmerzhafte Fasern mit kleinem Durchmesser. Um eine Deafferenzierung der Hornhaut und eine daraus resultierende Keratitis zu verhindern, ist die Elektrode so ausgerichtet, dass eine Schädigung des ersten Abschnitts des Trigeminusnervs vermieden wird. Ballonkompression und Glycerininjektion schädigen vorzugsweise große myelinisierte Fasern.
Mit diesen Techniken erfolgt eine sofortige Schmerzlinderung. Trigeminale sensorische Defizite sind bei Ballonkompression und Glycerininjektion normalerweise vorübergehend und nach Radiofrequenz-Thermokoagulation schwerwiegender und länger anhaltend.
Die Erzeugung einer Trigeminuswurzelläsion mit einem Gammamesser ist ein neueres Verfahren und wird durch mehrere Studien gestützt. Im Gegensatz zur sofortigen Schmerzlinderung, die mit perkutan verursachten Läsionen des Trigeminusganglions einhergeht, dauert es 6 bis 8 Wochen, bis sich die analgetische Wirkung der stereotaktischen Gammamesser-Radiochirurgie entfaltet. Ungefähr 24 bis 71 % der Patienten berichten 1 bis 2 Jahre nach dem Eingriff von einer anhaltenden Schmerzlinderung, und 33 bis 56 % berichten von einer anhaltenden Schmerzlinderung nach 4 bis 5 Jahren.
Bei 16 % der Patienten wurde über ein Taubheitsgefühl im Gesicht berichtet, während eine schmerzhafte Anästhesie praktisch nicht auftritt. Eine Metaanalyse ergab, dass etwa 34 % der Patienten nach einem Jahr keine Schmerzlinderung verspüren und wiederholte Eingriffe benötigen.
Mikrovaskuläre Dekompression
Die mikrovaskuläre Dekompression ist mittlerweile das chirurgische Verfahren der Wahl für die Mehrzahl der Fälle von Trigeminusneuralgie, die nicht auf Medikamente ansprechen.
Der Neurochirurg identifiziert das Gefäß, das die Wurzel des Trigeminusnervs komprimiert, bewegt es bei Bedarf von unterhalb des Nervs nach oberhalb des Nervs (siehe Abbildung unten) und führt normalerweise einen kleinen Schwamm ein, um die pulsierende Arterie von der Nervenwurzel getrennt zu halten.
Bei etwa 11 % der Patienten stellt der Chirurg keine neurovaskuläre Kompression oder minimalen Kontakt fest, ohne dass eine Nervenkompression erkennbar ist. In diesen Fällen setzt der Chirurg den Trennschwamm in der Regel trotzdem ein, allerdings ist die Misserfolgsrate höher als bei der Feststellung einer Nervenwurzeldistorsion. Dieses Problem unterstreicht den Vorteil der Verwendung etablierter MRT-Kriterien zur Identifizierung morphologischer Veränderungen in der Trigeminuswurzel.
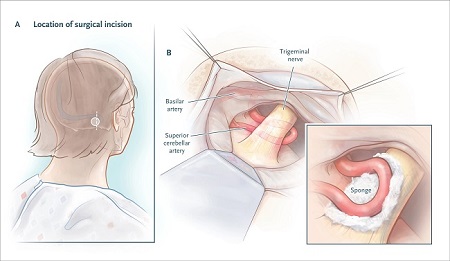
Mikrovaskuläre Dekompression.
Metaanalysen haben gezeigt, dass die mikrovaskuläre Dekompression der wirksamste chirurgische Eingriff bei klassischer Trigeminusneuralgie ist. 1 bis 2 Jahre nach dem Eingriff verspüren 68 bis 88 % der Patienten eine Schmerzlinderung und 61 bis 80 % haben nach 4 bis 5 Jahren eine Schmerzlinderung.
Die durchschnittliche Mortalität im Zusammenhang mit einer Operation beträgt 0,3 %. Liquorlecks treten bei 2,0 % der Patienten auf, Hirnstamminfarkte oder Hämatome bei 0,6 % und Meningitis bei 0,4 %.
Bei 2,9 % der Patienten kommt es zu einem teilweisen oder vollständigen Verlust der sensorischen Verteilung des Trigeminusnervs im Gesicht. Die besorgniserregendste Langzeitkomplikation, wenn auch selten (Inzidenz 1,8 %), ist der ipsilaterale Hörverlust.
Patienten mit Multipler Sklerose, die an einer arzneimittelresistenten Trigeminusneuralgie leiden, kann eine mikrovaskuläre Dekompression angeboten werden, obwohl die Evidenz hierfür unzureichend ist. Es wurde jedoch auch berichtet, dass sowohl perkutane Läsionen als auch Gammamesser-Läsionen bei Patienten mit Multipler Sklerose gute Ergebnisse erzielen.
Schlussfolgerungen
|















