Zusammenfassung
Hintergrund
Die Wirksamkeit der Therapeutika bei der Behandlung schwerer Erkrankungen, die durch SARS-CoV-2 verursacht werden, ist noch nicht erwiesen.
Methoden
Wir haben eine randomisierte, kontrollierte, offene Studie durchgeführt, an der hospitalisierte erwachsene Patienten mit bestätigter Infektion mit SARS-CoV-2, das die Atemwegserkrankung Covid-19 verursacht, und einer Sauerstoffsättigung (Sao2) von 94 % oder weniger beim Atmen teilnahmen Zimmertemperatur. . Luft oder ein Verhältnis des Sauerstoffpartialdrucks (Pao2) zum Anteil des eingeatmeten Sauerstoffs (Fio2) von weniger als 300 mm Hg.
Die Patienten wurden nach dem Zufallsprinzip im Verhältnis 1:1 einer Behandlung mit Lopinavir-Ritonavir (400 mg bzw. 100 mg) zweimal täglich über einen Zeitraum von 14 Tagen zusätzlich zur Standardversorgung oder allein der Standardversorgung zugeteilt.
Der primäre Endpunkt war die Zeit bis zur klinischen Besserung, definiert als die Zeit von der Randomisierung bis zu einer Verbesserung um zwei Punkte auf einer Ordnungsskala mit sieben Kategorien oder der Entlassung aus dem Krankenhaus, je nachdem, was zuerst eintrat.
Ergebnisse
Insgesamt 199 Patienten mit einer im Labor bestätigten SARS-CoV-2-Infektion wurden randomisiert; 99 wurden der Lopinavir-Ritonavir-Gruppe und 100 der Standardversorgungsgruppe zugeordnet.
Die Behandlung mit Lopinavir-Ritonavir war nicht mit einem Unterschied von der Standardbehandlung in der Zeit bis zur klinischen Besserung verbunden (Risikoverhältnis für klinische Besserung 1,24; 95 %-Konfidenzintervall [KI] 0,90 bis 1,72).
Die Mortalität nach 28 Tagen war in der Lopinavir-Ritonavir-Gruppe und in der Standardbehandlungsgruppe ähnlich (19,2 % vs. 25,0 %; Differenz –5,8 Prozentpunkte; 95 %-KI –17,3 bis 5,7) .
Der Prozentsatz der Patienten mit nachweisbarer viraler RNA war zu verschiedenen Zeitpunkten ähnlich.
In einer modifizierten Intention-to-Treat-Analyse führte Lopinavir-Ritonavir zu einer kürzeren mittleren klinischen Besserung von 1 Tag als bei der Standardbehandlung (Hazard Ratio 1,39; 95 %-KI 1,00 bis 1,91).
Gastrointestinale unerwünschte Ereignisse traten häufiger in der Lopinavir-Ritonavir-Gruppe auf, schwerwiegende unerwünschte Ereignisse traten jedoch häufiger in der Standardbehandlungsgruppe auf.
Die Behandlung mit Lopinavir-Ritonavir wurde bei 13 Patienten (13,8 %) aufgrund unerwünschter Ereignisse vorzeitig abgebrochen.
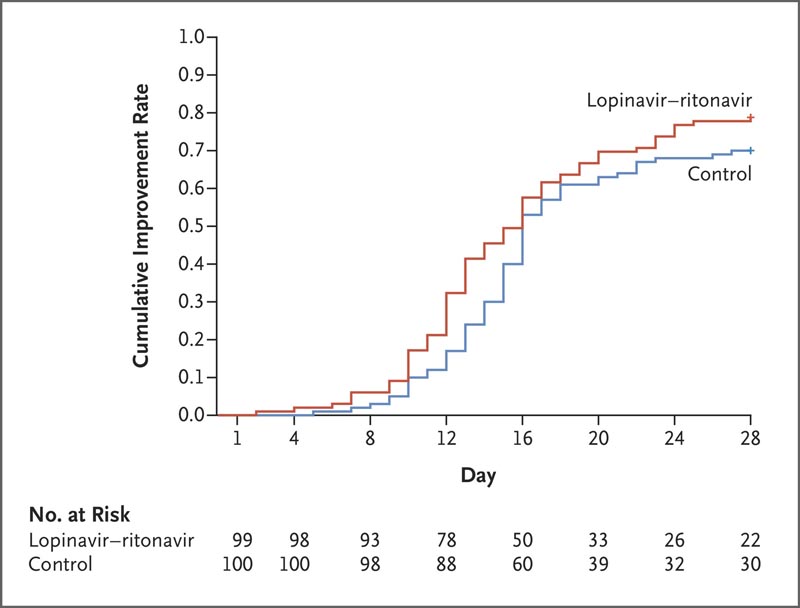
Zeit bis zur klinischen Verbesserung in der Intent-to-Treat-Population.
Diskussion
Diese randomisierte Studie ergab, dass die Behandlung mit Lopinavir-Ritonavir zusätzlich zur unterstützenden Standardbehandlung bei schwer erkrankten Patienten mit Covid-19 nicht mit einer anderen klinischen Verbesserung oder Mortalität verbunden war als mit der alleinigen Standardbehandlung.
Allerdings war in der modifizierten Intention-to-Treat-Analyse, die drei Patienten mit frühem Tod ausschloss, der Unterschied zwischen den Gruppen in der medianen Zeit bis zur klinischen Besserung (Median 15 Tage vs. 16 Tage) signifikant, wenn auch bescheiden.
Bemerkenswert ist, dass die Gesamtmortalität in dieser Studie (22,1 %) deutlich höher war als die 11 % bis 14,5 % Mortalität, die in ersten deskriptiven Studien mit hospitalisierten Patienten mit Covid-19 berichtet wurde,1,2, was darauf hindeutet, dass wir eine schwerkranke Population einbeziehen . Unsere Patientenpopulation war bei der Aufnahme in die Studie hinsichtlich Dauer und Schwere der Erkrankung heterogen;
Eine beschleunigte klinische Genesung (16,0 Tage gegenüber 17,0 Tagen) und eine verringerte Mortalität (19,0 % gegenüber 27,1 %) wurden in einer Post-hoc- Untergruppe der Patienten beobachtet, die innerhalb von 12 Tagen nach Auftreten der Symptome behandelt wurden, nicht jedoch bei den später behandelten Patienten. Die Frage, ob eine Vorbehandlung mit Lopinavir-Ritonavir bei Covid-19 einen klinischen Nutzen haben könnte, ist wichtig und bedarf weiterer Untersuchungen.
Der Befund steht im Einklang mit Studien, die zeigen, dass bei Patienten mit SARS-CoV-2-Viruspneumonie in der zweiten Krankheitswoche eine Progression auftritt, und mit Wirkungen, die in früheren antiviralen Studien bei SARS-COV2 und schwerer Grippe beobachtet wurden. . Darüber hinaus stellten wir fest, dass die Zahl der Lopinavir-Ritonavir-Empfänger, die schwere Komplikationen hatten (akute Nierenschädigung und Sekundärinfektionen) oder die wegen Atemversagens eine invasive oder nicht-invasive mechanische Beatmung benötigten, geringer war als bei denen, die keine Behandlung erhielten.
Diese Beobachtungen sind hypothesenführend und erfordern zusätzliche Studien, um festzustellen, ob die Behandlung mit Lopinavir-Ritonavir in einem bestimmten Krankheitsstadium einige Komplikationen bei Covid-19 reduzieren kann.
Wir haben nicht festgestellt, dass die zusätzliche Behandlung mit Lopinavir-Ritonavir die virale RNA-Belastung oder die Dauer der viralen RNA-Erkennbarkeit im Vergleich zur alleinigen unterstützenden Standardbehandlung verringert. Am Ende des Versuchs (Tag 28) wurde bei 40,7 % der Patienten in der Lopinavir-Ritonavir-Gruppe noch SARS-CoV-2-RNA nachgewiesen. Ein aktueller Bericht zeigte, dass die mittlere Dauer der Virusausscheidung bei Covid-19 bei Patienten mit schwerer Erkrankung 20 Tage betrug und bis zu 37 Tage dauern konnte.
Weder diese noch die aktuelle Studie fanden Hinweise darauf, dass Lopinavir-Ritonavir eine signifikante antivirale Wirkung ausübte. Die Gründe für den offensichtlichen Mangel an antiviraler Wirkung sind ungewiss, aber die in der aktuellen Studie verwendeten Probenahmemethoden waren wahrscheinlich nicht optimal. Proben wurden nur zeitweise entnommen (Tage 1, 5, 10, 14, 21 und 28), und eine häufigere Probenahme in den ersten 5 Tagen hätte zu einer detaillierteren Charakterisierung der Viruslastkinetik in den beiden Gruppen während dieses kritischen Zeitraums führen können .
Darüber hinaus haben frühere Studien gezeigt, dass Rachenabstrichproben eine geringere Viruslast aufweisen als Proben aus dem Nasopharynx, und was noch wichtiger ist, wir konnten keine Proben aus den unteren Atemwegen entnehmen.
Bemerkenswert ist, dass abhängig vom verwendeten Zelltyp die 50 % wirksamen Konzentrationen (EC50) von Lopinavir in vitro für SARS-CoV zwischen 4,0 und 10,7 μg pro Milliliter lagen, 5,6,8, obwohl andere Studien berichteten, dass Lopinavir inaktiv war26 Zur Hemmung waren mindestens höhere Konzentrationen (25 μg pro Milliliter) erforderlich.
Für MERS-CoV lagen die EC50-Werte zwischen 5 und etwa 7 μg pro Milliliter. Sowohl die mittlere Spitzenkonzentration (9,6 μg pro Milliliter) als auch die minimale Serumkonzentration (5,5 μg pro Milliliter) von Lopinavir bei Erwachsenen allein nähern sich diesen Konzentrationen an. Ob der EC50-Wert ein angemessener Schwellenwert ist und ob die Konzentrationen von ungebundenem Lopinavir im menschlichen Plasma für die Hemmung von SARS-CoV-2 ausreichen, ist fraglich.
Fast 14 % der Lopinavir-Ritonavir-Empfänger waren nicht in der Lage, die gesamte 14-tägige Verabreichungsdauer abzuschließen. Dies war hauptsächlich auf gastrointestinale unerwünschte Ereignisse zurückzuführen , darunter Anorexie, Übelkeit, Bauchbeschwerden oder Durchfall, sowie auf zwei schwerwiegende unerwünschte Ereignisse, beides akute Gastritis. Zwei Empfänger hatten selbstlimitierende Ausschläge.
Solche Nebenwirkungen, darunter das Risiko von Leberschäden, Pankreatitis, schwereren Hautausschlägen und QT-Verlängerung sowie die Möglichkeit mehrerer Arzneimittelwechselwirkungen aufgrund der CYP3A-Hemmung, sind bei dieser Arzneimittelkombination gut dokumentiert. Das in der aktuellen Studie beobachtete Nebenwirkungsprofil gibt Anlass zu Bedenken hinsichtlich der Verwendung höherer oder längerer Lopinavir-Ritonavir-Dosierungsschemata in dem Bemühen, die Ergebnisse zu verbessern.
Schlussfolgerungen
|
(Gefördert durch die National Major Science and Technology Projects on Creation and Development of New Drugs and other; Chinesische Registrierungsnummer für klinische Studien, ChiCTR2000029308. Öffnet in einem neuen Tab.)
















