Zusammenfassung Hintergrund Polyklonales Rekonvaleszentenplasma kann von Spendern gewonnen werden, die eine Coronavirus-Erkrankung 2019 (Covid-19) überstanden haben. Die Wirksamkeit dieses Plasmas bei der Vorbeugung schwerwiegender Komplikationen bei ambulanten Patienten mit kürzlich aufgetretenem Covid-19 ist ungewiss. Methoden In dieser multizentrischen, doppelblinden, randomisierten, kontrollierten Studie haben wir die Wirksamkeit und Sicherheit von Covid-19-Rekonvaleszentenplasma im Vergleich zu Kontrollplasma bei symptomatischen Erwachsenen (≥ 18 Jahre) bewertet, die positiv auf die schwere akute Atemwegserkrankung getestet wurden Coronavirus-2-Syndrom, unabhängig von ihren Risikofaktoren für das Fortschreiten der Krankheit oder ihrem Impfstatus. Die Teilnehmer wurden innerhalb von 8 Tagen nach Auftreten der Symptome aufgenommen und erhielten innerhalb eines Tages nach der Randomisierung eine Transfusion. Der primäre Endpunkt war ein Krankenhausaufenthalt im Zusammenhang mit Covid-19 innerhalb von 28 Tagen nach der Transfusion. Ergebnisse Die Teilnehmer wurden vom 3. Juni 2020 bis zum 1. Oktober 2021 eingeschrieben. Insgesamt wurden 1.225 Teilnehmer randomisiert und 1.181 erhielten eine Transfusion. In der vorab festgelegten modifizierten Intention-to-Treat-Analyse, die nur Teilnehmer umfasste, die eine Transfusion erhielten, trat das primäre Ergebnis bei 17 von 592 Teilnehmern (2,9 %) auf, die Rekonvaleszenzplasma erhielten, und bei 37 von 589 Teilnehmern (6,3 %), die Kontrollplasma erhielten ( absolute Risikoreduktion, 3,4 Prozentpunkte; 95 %-Konfidenzintervall, 1,0 bis 5,8; P = 0,005), was einer relativen Risikoreduktion von 54 % entspricht. Aus diesen Daten lassen sich keine Hinweise auf eine Wirksamkeit bei geimpften Teilnehmern ableiten, da 53 der 54 ins Krankenhaus eingelieferten Teilnehmer mit Covid-19 ungeimpft waren und 1 Teilnehmer teilweise geimpft war. Bei Teilnehmern, die nicht ins Krankenhaus eingeliefert wurden, traten insgesamt 16 unerwünschte Ereignisse vom Grad 3 oder 4 auf (7 in der Rekonvaleszenzplasmagruppe und 9 in der Kontrollplasmagruppe). Schlussfolgerungen Bei Teilnehmern mit Covid-19, von denen die meisten ungeimpft waren, verringerte die Verabreichung von Rekonvaleszentenplasma innerhalb von 9 Tagen nach Auftreten der Symptome das Risiko eines Fortschreitens der Krankheit, das zu einem Krankenhausaufenthalt führte. |
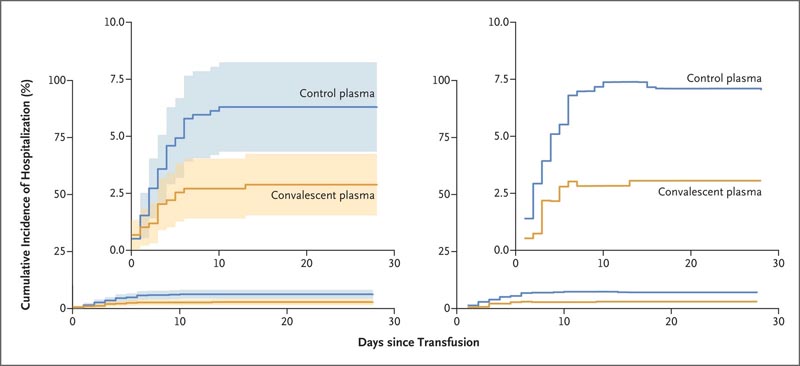
Kumulative Inzidenz von Krankenhauseinweisungen im Zusammenhang mit der Coronavirus-Erkrankung 2019. Die Ergebnisse der unbereinigten Analyse sind links dargestellt. Die Schattierung gibt das 95 %-Konfidenzintervall an. Rechts sind die Schätzungen gemäß dem Schätzmodell auf Basis angepasster minimaler fokussierter Verluste dargestellt. Die Kästchen zeigen dieselben Daten auf einer erweiterten Y-Achse.
Kommentare
Die von Experten begutachtete Veröffentlichung im New England Journal of Medicine bestätigt die erstmals im Dezember bekannt gegebenen Ergebnisse
Das New England Journal of Medicine (NEJM) veröffentlichte heute die endgültigen Ergebnisse einer landesweiten multizentrischen Studie unter der Leitung von Forschern der Johns Hopkins Medicine und der Johns Hopkins Bloomberg School of Public Health, in der Plasma von Patienten untersucht wurde, die sich von COVID-19 erholt haben und deren Blut enthält Antikörper gegen das verursachende Virus SARS-CoV-2 sind eine wirksame und sichere Möglichkeit zur frühzeitigen ambulanten Behandlung der Erkrankung.
Untersuchungen haben gezeigt, dass hochtitriges (antikörperreiches) COVID-Rekonvaleszenzplasma, wenn es an ambulante COVID-19-Patienten innerhalb von neun Tagen nach positivem Test verabreicht wurde, die Notwendigkeit einer Krankenhauseinweisung für mehr als die Hälfte der überwiegend ungeimpften ambulanten Patienten der Studie reduzierte.
Die US-amerikanische Food and Drug Administration (FDA) hat dieses Plasma derzeit als Behandlungsoption für ambulante Patienten mit immungeschwächten Erkrankungen oder unter immungeschwächten Medikamenten sowie für alle hospitalisierten Patienten mit COVID-19 im Frühstadium zugelassen.
Die Ergebnisse wurden erstmals in einem Preprint vorgestellt, der am 21. Dezember 2021 auf MedRxiv veröffentlicht wurde. Einzelheiten zur Studie, einschließlich Autoren und Finanzierungsquellen, finden Sie in der damals veröffentlichten Pressemitteilung von Johns Hopkins.
„Basierend auf unseren Erkenntnissen und Schlussfolgerungen, die nun durch den Peer-Review-Prozess validiert werden, ermutigen wir medizinisches Fachpersonal, SARS-CoV-2-antikörperreiches Blutplasma in ihren Blutbanken verfügbar zu halten.“ als Teil des Behandlungsarsenals gegen frühe Erkrankungen. „COVID-19-Stadium“, sagt der Co-Autor der Studie, David Sullivan, MD, Professor für molekulare Mikrobiologie und Immunologie an der Johns Hopkins Bloomberg School of Public Health mit einer gemeinsamen Berufung für Infektionskrankheiten an der Johns Hopkins University School of Medicine. .
„Wir glauben, dass die beste Rolle für Rekonvaleszenzplasma darin besteht, seinen Einsatz auf frühe ambulante Behandlungen auszudehnen, wenn andere Therapien, wie etwa monoklonale Antikörper oder Medikamente, nicht ohne weiteres verfügbar sind, wie etwa in Ländern mit niedrigem und mittlerem Einkommen, oder unwirksam sind, wie etwa in Ländern mit niedrigem und mittlerem Einkommen.“ „Es tritt bei Varianten von SARS-CoV-2 auf, die gegen bestimmte monoklonale Antikörper resistent sind“, fügt Sullivan hinzu.
In der ambulanten Frühbehandlungsstudie, die zwischen Juni 2020 und Oktober 2021 durchgeführt wurde, verabreichten Forscher 1.181 zufällig zugewiesenen Patienten eine Dosis polyklonales Rekonvaleszenzplasma mit hohem Titer (das eine konzentrierte Mischung aus SARS-spezifischen Antikörpern enthielt). CoV-2) oder Placebo-Kontrollplasma (ohne Antikörper gegen SARS-CoV-2). Die Patienten waren 18 Jahre oder älter und wurden innerhalb von acht Tagen vor der Transfusion positiv auf SARS-CoV-2 getestet. Eine erfolgreiche Therapie wurde definiert als ein Patient, der innerhalb von 28 Tagen nach der Plasmatransfusion keinen Krankenhausaufenthalt benötigte.
Die Studie ergab, dass 17 von 592 (2,9 %) Patienten, die Rekonvaleszenzplasma erhielten, innerhalb von 28 Tagen nach der Transfusion ins Krankenhaus eingeliefert werden mussten, verglichen mit 37 von 589 (6,3 %), die Placebo-Kontrollplasma erhielten. Dies führte zu einer relativen Risikoreduktion eines Krankenhausaufenthaltes um 54 %.
Auch der Zeitpunkt der Rekonvaleszenz-Plasmatransfusion ist entscheidend: „Je früher, desto besser“, sagen die Forscher.
„Basierend auf den Ergebnissen einer Analyse in der neuen Arbeit, die zum Zeitpunkt der Veröffentlichung des Vorabdrucks noch nicht verfügbar war, haben wir herausgefunden, dass die Wirksamkeit bei der Reduzierung von Krankenhausaufenthalten bei etwa 80 % liegt, wenn Rekonvaleszenzplasma innerhalb von fünf Tagen nach der Diagnose verabreicht wird.“ sagt Sullivan.
„Wir kommen zu dem Schluss, dass diese Ergebnisse stark dafür sprechen, dass SARS-CoV-2-Rekonvaleszenzplasma mit hohem Titer eine wirksame Frühbehandlung für COVID-19 ist und Vorteile wie niedrige Kosten, breite Verfügbarkeit und schnelle Resistenz gegen sich entwickelnde Varianten des Virus bietet“, sagt der Co-Senior-Autorin der Studie Kelly Gebo, MD, MPH, Professorin für Medizin an der Johns Hopkins University School of Medicine.
Der nächste Schritt besteht laut Forschern darin, Rekonvaleszentenplasma für die ambulante COVID-19-Behandlung einfacher nutzbar, effizienter zu verabreichen und für diejenigen, die es benötigen, zugänglicher zu machen. Im Rahmen dieser Bemühungen haben sie Ärzten Anleitungen für die Einrichtung eines ambulanten COVID-19-Plasmatransfusionszentrums gegeben, einschließlich der Anforderungen an Logistik, Personal und Blutbanken. Der Leitfaden erscheint in einem Artikel, der am 29. März 2022 in der Zeitschrift Transfusion veröffentlicht wurde.
Das Team strebt außerdem weiterhin nach einem besseren Verständnis darüber, was Rekonvaleszenzplasma sonst noch für ambulante Patienten mit COVID-19 leisten kann. In einer demnächst veröffentlichten Studie wird die Fähigkeit von Plasma untersucht, SARS-CoV-2-Varianten, einschließlich Delta und Omicron, zu neutralisieren, obwohl der Spender diesen Viren zuvor nicht ausgesetzt war.
Seit der ersten Bekanntgabe der Studienergebnisse im vergangenen Dezember gab es drei Entwicklungen, die den Einsatz von Rekonvaleszenzplasma bei COVID-19 im Frühstadium unterstützen:
- Am 28. Dezember 2021 erweiterte die FDA die genehmigte Notfallverwendung von Rekonvaleszentenplasma mit hohen Titern an Anti-SARS-CoV-2-Antikörpern „zur Behandlung von COVID-19 bei Patienten mit immunsuppressiver Erkrankung oder unter immunsuppressiver Behandlung, etwa in der …“ im ambulanten oder stationären Bereich.
- Am 2. Februar 2022 aktualisierte die Infectious Diseases Society of America ihre „Richtlinien für die Behandlung und Behandlung von Patienten mit COVID-19“ und enthielt nun auch die „Verwendung von Rekonvaleszenzplasma bei ambulanten Patienten mit leichter bis mittelschwerer COVID-19-Erkrankung mit hohem Progressionsrisiko“. zu einer schweren Erkrankung ohne andere Behandlungsmöglichkeiten.“
- Am 7. März 2022 gab das Amerikanische Rote Kreuz bekannt, dass es „vorübergehend alle Blutspenden auf COVID-19-Antikörper testet, um Spenden zu identifizieren, die zu Rekonvaleszenzplasma verarbeitet werden könnten“. Die Organisation sagte, dies werde getan, „um immungeschwächte Patienten zu unterstützen, die gegen COVID-19 kämpfen“.
„Diese jüngsten Erkenntnisse über den Nutzen von Rekonvaleszenzplasma mit hohem Titer bei der Behandlung von COVID-19 im Frühstadium sowie unsere von Experten überprüften Ergebnisse und unsere neuen Leitlinien für eine effektivere Behandlung bieten Ärzten eine zusätzliche Option für ambulante Patienten“, sagt er Gebo.