Hintergrund
Um das Risiko eines Fortschreitens der Coronavirus-Krankheit 2019 (Covid-19) zu verringern, sind neue Behandlungen erforderlich. Molnupiravir ist ein niedermolekulares orales antivirales Prodrug, das gegen das schwere akute respiratorische Syndrom Coronavirus 2 (SARS-CoV-2) wirksam ist.
Methoden
Wir führten eine doppelblinde, randomisierte, placebokontrollierte Phase-3-Studie durch, um die Wirksamkeit und Sicherheit einer Molnupiravir-Behandlung zu bewerten, die innerhalb von 5 Tagen nach Auftreten der Anzeichen oder Symptome bei nicht hospitalisierten, nicht geimpften Erwachsenen begonnen wurde. Im Labor wurde eine leichte bis mittelschwere Covid-19-Erkrankung und mindestens ein Risikofaktor für eine schwere Covid-19-Erkrankung bestätigt.
Die Teilnehmer der Studie erhielten nach dem Zufallsprinzip 5 Tage lang zweimal täglich 800 mg Molnupiravir oder Placebo.
Der primäre Wirksamkeitsendpunkt war die Häufigkeit von Krankenhausaufenthalten oder Todesfällen am Tag 29; Die Häufigkeit unerwünschter Ereignisse war der primäre Sicherheitsendpunkt.
Eine geplante Zwischenanalyse wurde durchgeführt, als 50 % der 1550 Teilnehmer (Zieleinschreibung) bis zum 29. Tag nachbeobachtet worden waren.
Ergebnisse
Insgesamt wurden 1433 Teilnehmer randomisiert; 716 erhielten Molnupiravir und 717 ein Placebo. Mit Ausnahme eines Ungleichgewichts beim Geschlecht waren die Ausgangsmerkmale in beiden Gruppen ähnlich.
Die Überlegenheit von Molnupiravir wurde in der Zwischenanalyse nachgewiesen; Das Risiko einer Krankenhauseinweisung jeglicher Ursache oder eines Todes bis zum 29. Tag war unter Molnupiravir (28 von 385 Teilnehmern [7,3 %]) geringer als unter Placebo (53 von 377 [14,1 %]) (Unterschied: –6,8 Prozentpunkte; 95 %-Konfidenzintervall). ). [KI], -11,3 bis -2,4; P = 0,001).
In der Analyse aller randomisierten Teilnehmer war der Prozentsatz der Teilnehmer, die bis zum 29. Tag ins Krankenhaus eingeliefert wurden oder starben, in der Molnupiravir-Gruppe niedriger als in der Placebo-Gruppe (6,8 % [48 von 709] vs. 9,7 % [68 von 699]. ]; Differenz –3,0 Prozentpunkte; 95 %-KI –5,9 bis –0,1).
Die Ergebnisse der Subgruppenanalysen stimmten weitgehend mit diesen Gesamtergebnissen überein; In einigen Untergruppen, etwa bei Patienten mit Anzeichen einer früheren SARS-CoV-2-Infektion, bei Patienten mit einer niedrigen Ausgangsviruslast und bei Patienten mit Diabetes, begünstigte die Punktschätzung der Differenz Placebo.
Bis zum 29. Tag wurde in der Molnupiravir-Gruppe ein Todesfall und in der Placebo-Gruppe neun Todesfälle gemeldet. Unerwünschte Ereignisse wurden bei 216 von 710 Teilnehmern (30,4 %) in der Molnupiravir-Gruppe und bei 231 von 701 (33,0 %) in der Placebo-Gruppe gemeldet.
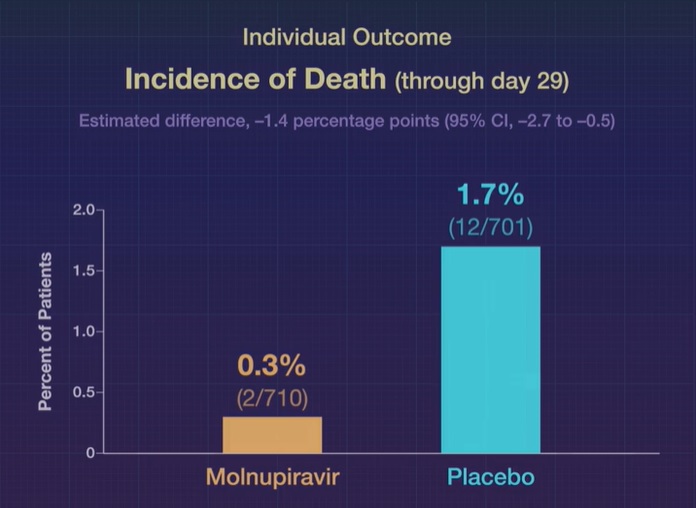
Schlussfolgerungen Eine frühzeitige Behandlung mit Molnupiravir verringerte das Risiko einer Krankenhauseinweisung oder eines Todesfalls bei ungeimpften und gefährdeten Erwachsenen mit Covid-19. |
(Gefördert von Merck Sharp und Dohme; MOVe-OUT ClinicalTrials.gov-Nummer, NCT04575597. Wird in neuem Tab geöffnet.)