Das Nationale Zentrum für Herz-Kreislauf-Forschung (CNIC) hat in Zusammenarbeit mit Wissenschaftlern aus Spanien und dem Ausland ein neues Diagnosetool entwickelt, das eine gleichzeitige Bewertung der elektrischen und mechanischen (kontraktilen) Aktivität des Herzens ermöglicht.
Zusammenfassung Die nicht-invasive elektromechanische Untersuchung bei Vorhofflimmern identifiziert zugrunde liegende Veränderungen der Vorhofmyopathie mit frühem prognostischem Wert Die elektromechanische Charakterisierung während Vorhofflimmerns (AF) bleibt eine große Lücke im Verständnis der AF-bedingten Vorhofmyopathie. Diese Studie liefert mechanistische Einblicke in den elektromechanischen Remodellierungsprozess , der mit dem Fortschreiten des Vorhofflimmerns verbunden ist, und demonstriert darüber hinaus dessen prognostischen Wert in der Klinik. Bei Schweinen zeigt die sequentielle elektromechanische Auswertung während des Vorhofflimmerns eine fortschreitende Abnahme der mechanischen Aktivität und eine frühe Dissoziation von ihrem elektrischen Gegenstück. Vorhofgewebeproben von Tieren mit Vorhofflimmern zeigen einen abnormalen Anstieg des Absterbens von Kardiomyozyten und Veränderungen in kalziumverarbeitenden Proteinen. Quantitative Hochdurchsatz-Proteomik- und Immunblot-Analysen in verschiedenen Stadien der AF-Progression identifizieren eine Herunterregulierung kontraktiler Proteine und einen fortschreitenden Anstieg der Vorhoffibrose. Darüber hinaus zeigen fortschrittliche optische Kartierungstechniken, die bei Vorhofflimmern auf Ganzherzpräparate angewendet werden, dass die durch Vorhofflimmern bedingte Umgestaltung die Frequenzschwelle für die Dissoziation zwischen Transmembranspannungssignalen und intrazellulären Kalziumtransienten im Vergleich zu gesunden Kontrollpersonen senkt. Auch Einzelzellsimulationen menschlicher Vorhof-Kardiomyozyten bestätigen die experimentellen Ergebnisse. Bei Patienten zeigt die nichtinvasive Beurteilung der atrialen elektromechanischen Beziehung weiter, dass die atriale elektromechanische Dissoziation ein früher prognostischer Indikator für die akute und langfristige Rhythmuskontrolle ist. Sie zeigen, dass der AF-bedingte Umbau die Frequenzschwelle für die Dissoziation zwischen Transmembranspannungssignalen und intrazellulären Kalziumtransienten im Vergleich zu gesunden Kontrollpersonen senkt. |
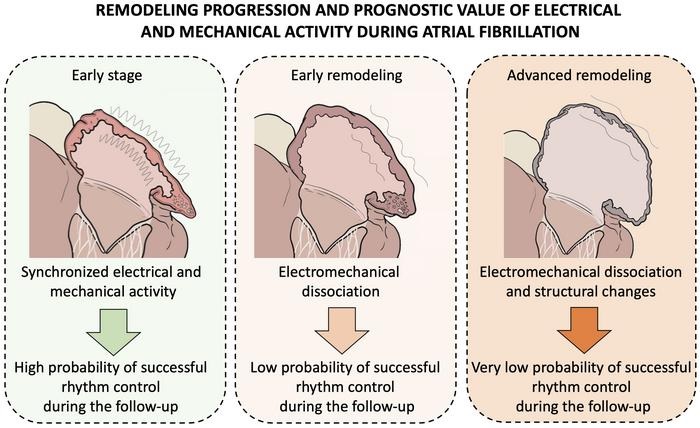
Abbildung : Schematische Darstellung des Fortschreitens der elektromechanischen Umgestaltung der Vorhöfe des Herzens während Vorhofflimmern, wobei in jedem Stadium der Erkrankung die Wahrscheinlichkeit der Wiederherstellung des normalen Rhythmus nach einer ununterbrochenen Episode von Vorhofflimmern angegeben wird.
Kommentare
Eine multidisziplinäre Studie unter der Leitung von Wissenschaftlern des National Center for Cardiocular Research (CNIC) stellt eine neue Methode zur Bewertung der strukturellen und elektrophysiologischen Veränderungen vor, die als atriale Umgestaltung bezeichnet werden und im Herzen von Patienten mit Vorhofflimmern, einer der häufigsten Formen von Vorhofflimmern, auftreten Arrhythmie. Die neue Diagnosemethode basiert auf der gleichzeitigen Auswertung der elektrischen und mechanischen (kontraktilen) Aktivität in den Vorhöfen des Herzens bei Vorhofflimmern. Die Studie wurde in Nature Communications veröffentlicht (DOI 10.1038/s41467-023-40196-y).
Der Leiter der Studie, David Filgueiras, erklärte, dass dies bisher „eine ungelöste Herausforderung“ sei, da einerseits „die verfügbare Technologie es nicht zuließ, beide Arten von Informationen zu integrieren, um eine umfassendere Bewertung zu ermöglichen“. Und andererseits: „Bei Vorhofflimmern sind die kontraktilen Bewegungen der Vorhöfe von geringer Intensität und ihre Messung stellt eine technische Herausforderung dar.“ Vorhofflimmern ist ein unregelmäßiger und oft sehr schneller Herzschlag, der zur Bildung von Blutgerinnseln im Herzen führen kann, was das Risiko eines Schlaganfalls, einer Herzinsuffizienz und damit verbundener Komplikationen erhöht. Von Vorhofflimmern sind in Europa etwa 10 Millionen Menschen und in Spanien etwa 700.000 Menschen betroffen.
Vorhofflimmern wird derzeit danach klassifiziert, wie lange der Patient schon an Herzrhythmusstörungen leidet. Allerdings erklärt Dr. Filgueiras, der die Gruppe „Advanced Development in Arrhythmia Mechanisms and Therapy“ am CNIC leitet und Kardiologe am Health Research Institute des San Carlos Clinical Hospital (IdISSC) ist, „diese zeitliche Klassifizierung liefert keine Informationen über die.“ Status eines Patienten oder der Grad der Vorhofumgestaltung , ein besonders wichtiger Parameter in den ersten Monaten der Erkrankung, wenn die zugrunde liegenden Krankheitsprozesse unterschiedlich schnell fortschreiten können.
Laut Dr. Filgueiras „liegt die Bedeutung dieser neuen Diagnosemethode in ihrer Fähigkeit, eine personalisierte Beurteilung des Grades der Vorhofumgestaltung eines einzelnen Patienten zu ermöglichen, unabhängig von der klinischen Klassifizierung auf der Grundlage zeitlicher Kriterien.“
Die ersten drei Autoren der Studie sind Daniel Enríquez Vázquez vom Universitätsklinikum A Coruña und Mitglied des spanischen Netzwerks für kardiovaskuläre Forschung (CIBERCV) sowie die CNIC-Wissenschaftler Jorge G. Quintanilla und Alba García Escolano. Dr. Enríquez Vázquez betonte: „Auf klinischer Ebene zeigen die Ergebnisse, dass die elektromechanische Dissoziation bei Patienten mit Vorhofflimmern ein solider Indikator für das Fortschreiten der Krankheit und die Notwendigkeit ist, dringend Maßnahmen zu ergreifen, um diese Patienten wieder in einen normalen Rhythmus zu bringen.“ effizient und stabil. Benehmen."
Das von Dr. Filgueiras geleitete Team arbeitete in Zusammenarbeit mit Kollegen des San Carlos Clinical Hospital, des Central University Hospital of Asturias, des Hospital de la Santa Creu i Sant Pau, des University Hospital Complex of A Coruña, der Complutense University of Madrid, die Polytechnische Universität Madrid, die Autonome Universität Barcelona, die University of Connecticut und das CIBERCV. In den letzten 10 Jahren hat dieses Team aus nationalen und internationalen Experten zusammengearbeitet, um elektrische und mechanische Herzdaten zu integrieren, um eine personalisierte Charakterisierung des Status pathologischer Veränderungen im Zusammenhang mit dem Fortschreiten des Vorhofflimmerns zu ermöglichen.
Dieses vielfältige Team konnte dies durch einen multidisziplinären Ansatz erreichen.
In der ersten Phase entwickelten Ingenieure und Physiker die am besten geeignete Strategie zur Integration elektrischer und mechanischer Daten . Die gefundene Lösung bestand darin, die mechanische Aktivität mithilfe der Doppler-Bildgebung zu messen, einer nicht-invasiven Methode, die Informationen über Vorhofgewebebewegungen liefert, und die elektrische Aktivität mithilfe der Oberflächenelektrokardiographie.
Beide Ansätze lassen sich in der Klinik leicht umsetzen, da sie nicht-invasiv sind und im Rahmen einer transthorakalen Ultraschalluntersuchung, einer Routineuntersuchung der Form und Funktion des Herzens und einiger seiner inneren Strukturen, durchgeführt werden können.
An der zweiten Phase nahmen Experten aus Biologie, Biotechnologie, Biochemie und biomedizinischer Technik teil und arbeiteten mit der CNIC Proteomics Unit und klinischen Kardiologen zusammen. In dieser Phase durchgeführte experimentelle Studien korrelierten die mit dem neuen Ansatz gewonnenen Informationen mit den zugrunde liegenden pathologischen Veränderungen im Ohrmuschelgewebe. Diese Informationen wurden verwendet, um neue fortschrittliche Kartierungstechniken und Computersimulationen zu entwickeln, um die Mechanismen aufzudecken, die der elektrischen und mechanischen Umgestaltung während des Vorhofflimmerns zugrunde liegen.
Die letzte Phase war eine prospektive multizentrische Studie mit 83 Patienten in einem frühen Stadium der Entwicklung von Vorhofflimmern, um den prognostischen Wert einer gleichzeitigen elektrischen und mechanischen Beurteilung der Vorhöfe bei Patienten mit dieser Art von Arrhythmie zu bestimmen.
Experimentelle und klinische Befunde zeigten ein Ungleichgewicht zwischen elektrischer und mechanischer (kontraktiler) Aktivierung in den Vorhöfen im Frühstadium der Erkrankung. Dies führt dazu, dass die beiden Parameter dissoziieren , sodass die kontraktile Aktivierung nicht mit der elektrischen Aktivierung Schritt halten kann, ein Phänomen, das Forscher als atriale elektromechanische Dissoziation bezeichnen . Der Rhythmus dieser Dissoziation ist individuell für den einzelnen Patienten, wird jedoch bei fehlender Wiederherstellung des normalen Rhythmus normalerweise innerhalb der ersten 2–3 Monate nach einer ununterbrochenen Episode von Vorhofflimmern beobachtet.
Ein wesentlicher Vorteil des neuen Ansatzes besteht darin, dass die elektromechanische Dissoziation des Vorhofs erkannt wird, bevor offensichtliche klinische Anzeichen einer strukturellen Vorhofumgestaltung auftreten . „Der Einsatz dieses neuen diagnostischen Ansatzes ermöglicht eine frühzeitige Charakterisierung des zugrunde liegenden Umbaus bei Patienten mit Vorhofflimmern“, sagte Dr. Filgueiras. „Die Studie zeigt, dass es möglich ist, elektrische und mechanische Daten aus den Vorhöfen von Patienten mit Vorhofflimmern zu integrieren, um personalisierte prognostische Informationen über den klinischen Verlauf der Krankheit zu erhalten.“
Nicasio Pérez Castellano vom IdISSC und David Calvo Cuervo vom Zentralkrankenhaus von Asturien und derzeit Mitglied des IdISSC betonten, dass „neben den erzielten Ergebnissen eine große Stärke dieses neuen Ansatzes darin liegt, dass er nicht invasiv ist.“ Natur, was das Management erheblich erleichtert.“ von Patienten mit Vorhofflimmern.
Julián Pérez Villacastín, klinischer Mitarbeiter der Studie am Hospital Clínico San Carlos, CIBERCV und derzeit Präsident der Spanischen Gesellschaft für Kardiologie, fügte hinzu, dass „diese Forschung und ihre klinische Umsetzung eine zunehmend personalisierte Behandlung von Patienten mit Vorhofflimmern ermöglichen werden.“
Die Studie wurde vom H2020-Programm der Europäischen Union (Grant Agreement Nr. 965286), dem Ministerium für Wissenschaft und Innovation (PID2019-109329RB-I00 und PGC2018-097019-B-I00) und dem Carlos III Health Institute (Europäischer Fonds für Gesundheitsforschung) finanziert PRB3 (PT17/0019/0003-ISCIII-SGEFI/FEDER, ProteoRed), Interhospital Fund for Cardiovascular Research, CIBERCV, Fundación Salud 2000 und Fundación La Caixa (Projektcode HR17-00247).















